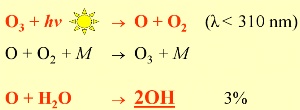> magyar > Climate Encyclopaedia > Alsó légkör > Haladó > 1. Oxidánsok & Megfigyelések > - oxidáció & OH
> magyar > Climate Encyclopaedia > Alsó légkör > Haladó > 1. Oxidánsok & Megfigyelések > - oxidáció & OH
|
Alsó légkörHaladó
|
Oxidáció a légkörbenSzámos kémiai vegyület jut a légkörbe, és felhalmozódna, ha ismételten nem kerülne onnan ki. A kiülepedés történhet száraz ülepedéssel, vagy esõ révén (nedves ülepedés). Különösen a gáznemû szerves vegyületek kerülnek ki a légkörbõl könnyen, ha átalakulnak kevésbé illékony, vízoldható oxidált állapotba
|
|
Az oxidáció kémiai értelemben nem szükségszerûen jelent egy oxigént tartalmazó molekulával való reakciót. De a levegõ a legtöbb esetben oxigént is tartalmaz. Három fõ oxidáns van, ami az ilyen jellegû folyamatokat irányítja a légkörben: A hidroxil gyök OH
|
|
Hogyan képzõdik az OH?Az OH irányítja a légköri kémiát a nap folyamán, mert képzõdése elsõsorban a Napból érkezõ sugárzástól függ. A kezdõ reakció (fent) a napfény hatására történõ ózonbomlás (fotolízis), ami 310 nm-nél rövidebb hullámhosszú sugárzás hatására játszódik le, majd ezt követi a kialakult oxigén atom reakciója a vízzel. Ezért egy bizonyos mennyiségû troposzférikus ózon alapvetõ a troposzféra kémiájához, habár a túl sok nem egészséges.
|
Mennyi OH képzõdik?Mivel az OH rendkívül reagens gyök, kialakulása után azon nyomban reakcióba lép. Élettartama körülbelül egy másodperc vagy még kevesebb. Ez azt jelenti, hogy a koncentrációja nagyon alacsony, 1x105 és 2x107 molekula cm-3 között. Tengerszinti nyomáson ez 0.01 - 1 ppt (pmol/mol) keverési arányt jelent. |
|
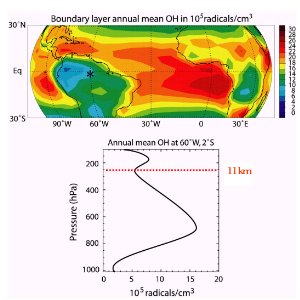
De különösen a szélességgel csökken, mert nem csak a nedvességtartalom csökken, hanem a sarkok felé a napfénytartam és intetnzitás is. Hogyan lép az OH reakcióba?A jobboldalon lévõ kép egy érdekes hatást mutat trópusi esõerdõk fölött. Az OH koncentráció csökken a talaj közelében. Mi ennek az oka? Az erdõk sok szerves vegyületet, mindenek elõtt izoprént bocsátanak ki, és az reakcióba lép az OH-val. Ezért van az erõs OH koncentráció-csökkentõ folyamat a talajhoz közel. A kémiai reakciók használják fel. Az OH-nak nagy affinitása van a szerves vegyületekbõl, RH, elvonja a hidrogént amikor csak lehetséges, és vizet H2O hoz létre. A következõ lépésben az R
|
|
|
Azonban, az OH világszerte elsõsorban nem az erdõkbõl származó szerves vegyületekkel lép reakcióba. A szerves gázok 30%-kal, a metán (a legfontosabb és a legkisebb szerves molekula) további 15%-kal járul hozzá az OH eltávolításhoz. A gáz, ami leginkább reakcióba lép az OH-val a szénmonoxid (40%) és a fennmaradó 15%-ban az ózonnal, O3, hidroperoxil gyökkel, HO2 és hidrogénnel, H2, lép reakcióba.
|
|
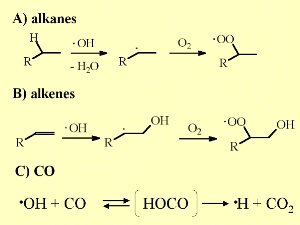
Az OH igyekszik kialakítani kétszeres kötést kölcsönhatásában a kicsi alkénekkel, a szerves vegyületek speciális osztályával, addig, míg a telített maradék nem sokkal nagyobb és a H elvonás statisztikailag megfelelõ. Itt peroxid képzõdés is elõfordul.Az OH képes oxidálni a szénmonoxidot, CO, széndioxiddá CO2. Amint láttuk a CO és a metán, CH4, a fõ OH nyelõk. Más reagens szerves vegyületek csak nyomokban, néhány ppt mennyiségben fordulnak elõ, amíg a CO átlagos szintje eléri a 120 ppb-t az északi féltekén (több égési folyamat) és a 60 ppb-t a déli féltekén.
|
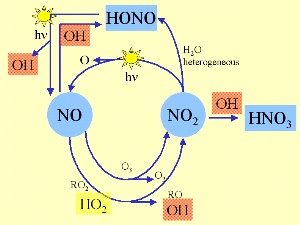
Habár az OH a legfontosabb oxidáns a légkörben, az éjszakai koncentrációja közel van a nullához, mert a napfény szükséges a képzõdéséhez. Ezért a sötétben és az éjszaka a nitrátok, NO3, és az ózon O3, kémiája sokkal fontosabbá válik.
|
|
* A keverési arányt ppb-t és ppm-t (= 1 molekula 1 milliárd közül vagy 1 molekula 1 millió közül) gyakran használják tudományos publikációkban, illetve más légköri és éghajlati irodalomban is. Mi is használtuk az Éghajlati Enciklopédiában. Azonban, sokkal helyesebb az 1 nmol/mol (= 1 ppb) vagy 1 µmol/mol (= 1 ppm). Ugyanis a molekulák mennyiségének, n-nek a mértékegysége a mol.
|
Az oldalról:szerzõ: Dr. Elmar Uherek - Max Planck Institute for Chemistry, Mainz
|