> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 1. Oxidation und Beobachtung > - Nacht & Nitrat
> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 1. Oxidation und Beobachtung > - Nacht & Nitrat
|
Untere AtmosphäreMehr |
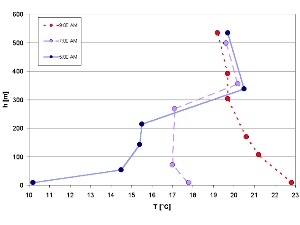
Nächtliche Bedingungen und ChemieDie Chemie, die in der Atmosphäre stattfindet, hängt nicht nur davon ab, welche Verbindungen in sie entlassen werden, sondern auch davon, welche Bedingungen in ihr herrschen. Letztere sind durch die Jahreszeiten bestimmt, durch den Wechsel von Tag und Nacht, durch Temperaturprofile, durch die Feuchte und anderes mehr.
|
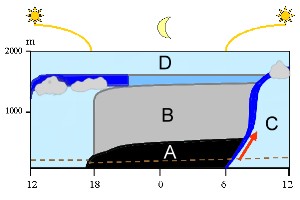
Nächtliche Inversion in der planetaren GrenzschichtAlles, was sich an Luft unterhalb der freien Atmosphäre (D) befindet, gehört zur planetaren (erdnahen) Grenzschicht. In dieser ändern sich im Verlauf eines Tages die Bedingungen (von links nach rechts): Zum Mittag ist die Luft durchmischt (hellblau). Nach Sonnenuntergang bildet sich die stabile nächtliche Schicht aus (A) und die übrige Luft lagert über ihr (B). Die Luft der Oberflächenschicht unterhalb der gepunkteten Linie kann während der Nacht nicht in höhere Lagen aufsteigen. Hierzu fehlt die antreibende Energie. Diese wird erst wieder mit dem Sonnenaufgang verfügbar. Der Erdboden erwärmt sich, die warme (= leichtere) Luft beginnt zu steigen (roter Pfeil), die stabile Schichtung der Nacht bricht auf. Eine Luft mit sich führende Schicht (engl.: entrainment zone) steigt vom Erdboden bis in die höchsten Lagen der planetaren Grenzschicht auf (dunkelblau) und führt zu einer Durchmischung der Luft während des Tages (C).
|
|
Im Winter kann es vorkommen, dass die Sonne über einen oder auch mehrere Tage nicht stark genug ist, die Inversionsschicht aufzulösen. In solchen Fällen sammeln sich die Abgase und Verschmutzungen über den Städten und führen zu Smog. Besondere Bedingungen findet man auch oft in Gebirgstälern, wie auf dem Photo rechts gezeigt. Die Inversion bleibt unterhalb einer Wolkendecke bestehen.
|
|
|
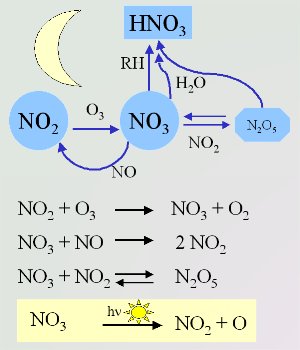
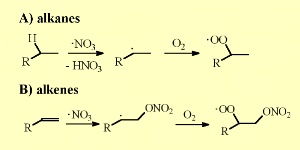
NitratchemieAuf Grund der unterschiedlichen Bedingungen während der Nacht ist auch die Chemie anders. Es gibt weniger Quellen für OH. Nitratradikale gehen stattdessen während der Nacht ähnliche Reaktionen ein, wie es OH während des Tages tut. Nitratradikale NO3 entstehen aus der Reaktion von Ozon mit Stickstoffdioxid (Basis Einheit 3). Mit NO reagieren sie wieder zurück. Daher können NO und NO3 in höheren Konzentrationen nicht gemeinsam vorhanden sein. Die Reaktion von NO2 und NO3 ist der einzige Weg in der Atmosphäre zur Bildung von Distickstoffpentoxid N2O5. Dieses kann sich in Wasser zu Salpetersäure zersetzen oder zu den Ausgangsverbindungen (Edukten) zurückreagieren. Wie auch OH, so spalten Nitratradikale von Alkanen ein H-Atom ab. Salpetersäure HNO3 und ein Alkylradikal R
|
NO3 addiert sich auch an die Doppelbindungen von ungesättigten organischen Verbindungen und bildet Peroxynitrate nach weiterer Reaktion mit O2.
|
|
|
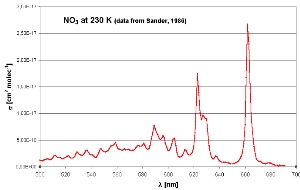
NO3 absorbiert Licht im roten Bereich des sichtbaren Spektrums. Sobald es am Ende der Nacht hell wird, wird es vom ersten Licht gespalten, vor allem in NO2 und O. Die OH-Chemie des Tages dominiert wieder. Ozon, das dritte wichtige Oxidationsmittel in der Atmosphäre, kann nicht mit Alkanen reagieren. Aber es ist eine Konkurrenz für OH in der Reaktion mit Alkenen, wenn es relativ dunkel ist, z.B. am Abend oder im Winter. Ein spezielles Kapitel erklärt die Ozonreaktionen näher.
|
|