> Polski > Climate Encyclopaedia > Troposfera > więcej > 1. Utlenianie i pomiary > - noc i azotany
> Polski > Climate Encyclopaedia > Troposfera > więcej > 1. Utlenianie i pomiary > - noc i azotany
|
TroposferaDowiedz się więcej! |
Procesy chemiczne zachodzące w atmosferze nocąProcesy chemiczne zachodzące w atmosferze zależą nie tylko od rodzaju związków emitowanych do powietrza, ale także od warunków meteorologicznych. Te zaś zależą m.in. od pory roku i dnia, a określamy je opisując np. temperaturę czy wilgotność powietrza.
|
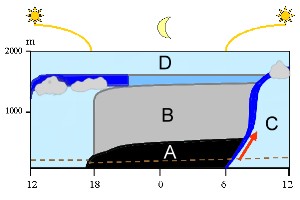
Nocna inwersja temperatury w planetarnej warstwie granicznej Masy powietrza znajdujące się poniżej swobodnej atmosfery (oznaczonej jako D na ryc. 2) należą do planetarnej warstwy granicznej. Zmiany niektórych jej cech zachodzą w ciągu doby (od lewej do prawej na ryc. 2): w południe powietrze jest wymieszane (kolor jasnoniebieski). Po zachodzie Słońca tworzy się w dolnej warstwie atmosfery nocna warstwa stałej równowagi atmosfery (A), a powyżej znajduje się nocna warstwa słabej turbulencji (B). Powietrze znajdujące się w warstwie przygruntowej (poniżej przerywanej brązowej linii) nie może w nocy przemieszczać się do wyższych warstw atmosfery. Brak energii słonecznej, która wyzwala ten proces. Nad ranem ziemia zaczyna się ogrzewać, powietrze zaczyna się unosić (czerwona strzałka), nocna warstwa stałej równowagi zaczyna zanikać. Tworzy się wąska tzw. strefa wznoszenia (ciemny niebieski kolor), która unosi się stopniowo aż do górnej granicy planetarnej warstwy granicznej i pozostawia poniżej w ciągu dnia konwekcyjną warstwę mieszania (C). |
|
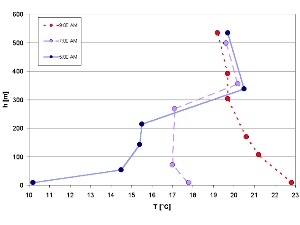
Zimą zdarza się, że Słońce jest zbyt nisko ponad horyzontem aby warstwa inwersyjna mogła zaniknąć. Utrzymuje się ona więc przez cały dzień, a nawet kilka dni. Jeśli ma to miejsce nad miastem to zanieczyszczenie powietrza gromadzi się w powietrzu i może to doprowadzić do powstania smogu. W górach zimą warunki meteorologiczne są szczególne, a inwersja może utrzymywać się np. pod warstwą chmur wypełniającą dolinę (ryc.3). |
|
|
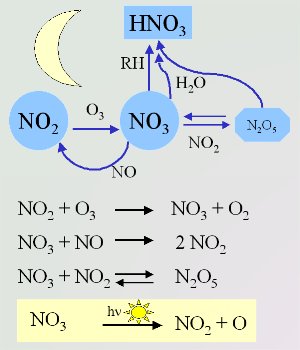
Reakcje chemiczne z udziałem azotanówTo, że warunki meteorologiczne są w nocy inne niż w ciągu dnia powoduje, że procesy chemiczne zachodzące w atmosferze także są inne. Jest dostępne mniej źródeł OH, a rodniki azotanowe wchodzą w podobne reakcje z gatunkami organicznymi jak OH w ciągu dnia. Rodniki azotanowe NO3 tworzą się wskutek reakcji ozonu O3 z dwutlenkiem azotu NO2 (patrz: poziom „podstawy”, część 3). Następnie, przy udziale NO, zachodzi reakcja prowadząca do ponownego powstania NO2. To z tego powodu NO i NO3 nie mogą występować łącznie w wysokich stężeniach. Reakcja między NO3 i NO2 jest jedynym sposobem powstawania N2O5 w atmosferze. Może on albo ulec hydrolizie w wodzie albo rozpaść się z powrotem na NO2 i NO3.
|
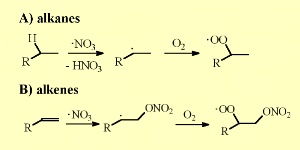
NO3 także dołącza się do podwójnych wiązań nienasyconych związków organicznych i tworzy azotany nadtlenowe po dodaniu O2. Co ciekawe, czas przebywania NO3 / N2O5 w atmosferze drastycznie spada wraz ze wzrostem zawartości pary wodnej. HNO3 tworzy się wskutek reakcji z wodą, zwłaszcza gdy jest to cienka jej warstwa na jakiejś powierzchni..
|
|
|
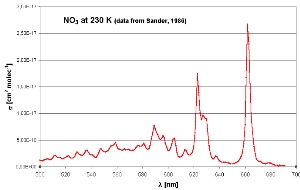
NO3 pochłania światło w czerwonej części widma widzialnego. Wraz z pierwszymi promieniami Słońca, ulega fotolizie głównie do NO2 i O, a reakcje z udziałem OH- ponownie dominują. Ozon, trzeci ważny utleniacz w atmosferze, nie jest w stanie reagować z alkanami, ale może stanowić konkurencję dla alkenów jeśli stężenie OH obniży się w warunkach niedoboru światła (zimą albo wieczorem). Reakcje z udziałem ozonu są opisane w osobnym tekście. |
|
Zajrzyj także na te strony! Więcej informacji o tlenkach azotu w powietrzu:
|
O tej stronie:
|