> Deutsch > Climate Encyclopaedia > Obere Atmosphäre > Mehr > 2. Ozon > - Chlorchemie
> Deutsch > Climate Encyclopaedia > Obere Atmosphäre > Mehr > 2. Ozon > - Chlorchemie
|
Obere AtmosphäreMehr .. |
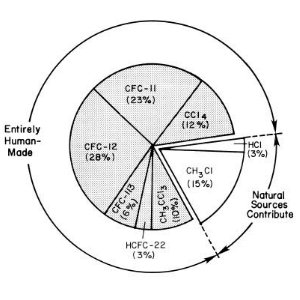
ChlorchemieVor allem die Chlorchemie treibt die Zerstörung der Ozonschicht an. Mit der industriellen Produktion der Fluorchlorkohlenwasserstoffe (FCKW) brachte der Mensch eine völlig neue Spezies von Chlorverbindungen in die Atmosphäre. Chlorverbindungen sind heute um das Sechsfache höher konzentriert als von Natur aus, mit fatalen Folgen für die Ozonschicht. Die Bedingungen für die Bildung des Ozonloches über der Antarktis allerdings sind ganz besondere. Von daher wurde auch eine so drastische Entwicklung nicht vorhergesehen.
|
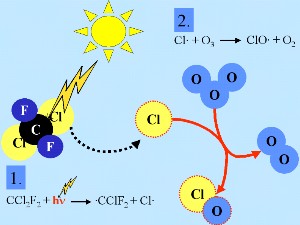
Stratosphärische Chlorchemie
|
| X |
-> XO | |
| O3 + Licht | -> O + O2 | |
| O + XO |
-> X | |
| netto: | 2 O3 | -> 3 O2 |
Diese Kettenreaktion treibt den Ozonabbau an.
 |
|
2. a) Grundlagen der stratosphärischen Chlorchemie
|
Das die Kette auslösende Radikal X
|
|
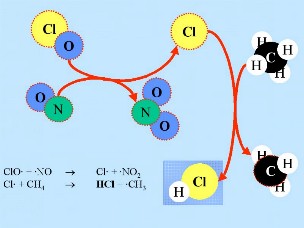
HCl und ClONO2 sind sogenannte 'Reservoir Spezies', da in ihnen Chlor nicht aktiv ist sondern zwischengelagert. Solche Spezies reagieren nicht mit Ozon. Sie verbleiben normalerweise in der Gasphase und können nach und nach wieder aus der Stratosphäre entfernt werden. Daher ist in der normalen stratosphärischen Gasphasenchemie nur ein leichter Ozonabbau zu erwarten. Doch werden diese Spezies mit der allgemeinen Zirkulation in die untere Stratosphäre der Gebiete im polaren Winter transportiert ...
|
|
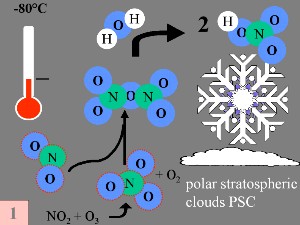
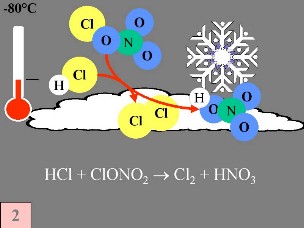
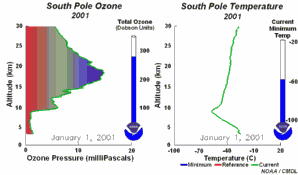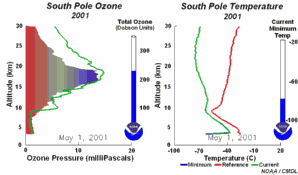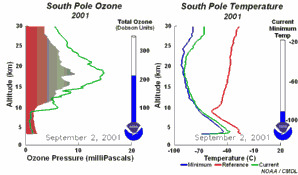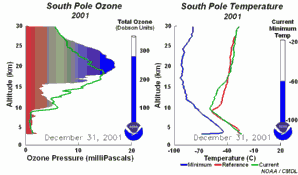
Die speziellen Bedingungen des Ozonloches über der AntarktisWährend der Polarnacht mit Temperaturen von etwa -80°C beginnen selbst die letzten Spuren von Wasser, die in der Stratosphäre verfügbar sind, zu gefrieren. Sie bilden zusammen mit Salpetersäure polare stratosphärische Eiswolken (sogenanntes Salpetersäuretrihydrat -> nitric acid trihydrate NAT). Nun können fünf Schlüsselbedingungen zusammenkommen.
|
|
Erstens: Die Stickoxidkatalysatoren (Stickstoffmonoxid NO und Stickstoffdioxid NO2), die dabei helfen, ClO
Die hierbei erzeugte Salpetersäure HNO3 wird in die Eisteilchen der polaren Stratosphärenwolken (polar stratospheric clouds PSC) eingeschlossen.
|
|
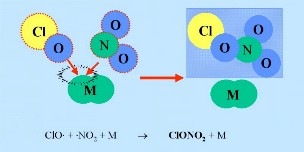
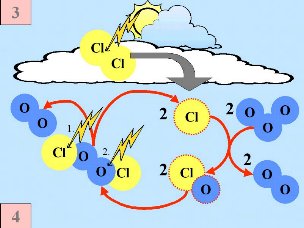
Zweitens: Auf der Oberfläche der PSC bildenden Eispartikel reagieren die 'Reservoir Spezies' HCl und ClONO2 miteinander und erzeugen Cl2 und HNO3; letztere wird sofort in die Partikel eingebaut. Drittens: Nach Ende der Polarnacht und der Rückkehr des Tageslichtes wird Chlor Cl2 durch das Sonnenlicht gespalten (photolysiert) und erzeugt 2 Cl
|
|
Viertens: Die Chloratome lösen eine katalytische Kette von Reaktionen aus, die zu einem Abbau des Ozons führt, solang keine Stickoxide verfügbar werden, die die Chlorradikale abfangen. Man beachte, dass die Geschwindigkeit des Ozonabbaus quadratisch mit der Konzentration an Cl Cl |
|
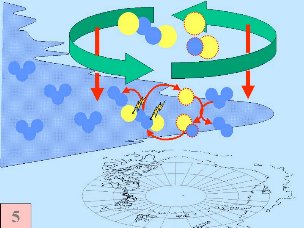
Fünftens: Normalerweise werden Chlorspezies wie Cl
|
Alle fünf Bedingungen müssen zusammenkommen, um einen sehr starken Ozonabbau wie im Ozonloch zu bewirken. Daher erfolgt der gravierendste Abbau über der Antarktis und ausschließlich in den Monaten September / Oktober des antarktischen Frühlings am Ende der Polarnacht. In manchen Jahren stellen sich ähnliche Bedingungen auch im März über der Arktis ein und ein kleineres Ozonloch bildet sich über Nordeuropa. Später im Jahr lösen sich die Polarwolken auf, Stickoxide werden wieder verfügbar und der Polarwirbel bricht zusammen. Dann werden die Chlorradikale anderweitig abgefangen und die Ozonschicht erholt sich wieder.
|
|
______________
|
|
|