> Español > Climate Encyclopaedia > estratosfera > Más > 2. Ozono > - Ozono estratosférico
> Español > Climate Encyclopaedia > estratosfera > Más > 2. Ozono > - Ozono estratosférico
|
Alta AtmósferaSaber más
|
La química del ozono estratosféricoFue fundamentalmente después de 1980 cuando nuestro conocimiento sobre la química del ozono estratosférico creció mucho. La razón fue el descubrimiento del agujero de la capa de ozono en 1985. Las dos secciones siguientes dan una visión global de la química de la estratosfera en su marco histórico.
|
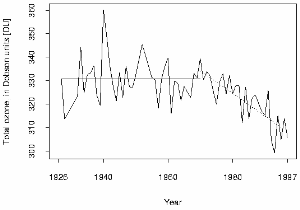
Descubrimiento del ozono y primeras medidasLa investigación del ozono es una rama bastante antigua de la ciencia atmosférica. En 1840 el gas fue bautizado como "ozono" (el olor) por el químico Christian Friedrich Schönbein, quien descubrió que esta sustancia se formaba durante descargas eléctricas. Muy pronto se descubrió que el ozono era un componente natural del aire. El primer método de medida de este gas lo desarrolló el propio Schönbein, pero muy pronto fue mejorado en el Observatorio Mt. Souris de Paris. De ahí vienen las primeras series de datos (1876 - 1910) que hoy son la mejor aproximación de las concentraciones preindustriales de la capa fronteriza.
|
|
|
En 1879 se descubrió que la región UVB del espectro solar disminuye significativamente en la superficie de la Tierra y en 1880 se supo que el ozono es un fuerte absorbente en este rango, y por ello podría ser el responsable. Sin embargo, la cantidad de ozono disponible en la baja troposfera no puede explicar esta disminución. Por ello se ha asumido que la mayor parte del ozono tiene que formarse en capas altas de la atmósfera. La investigación clave fue llevada a cabo por Gordon Dobson en los años 20 del siglo XX. Desarrolló el espectrómetro Dobson que se ha utilizado desde 1929 para medir la columna de ozono total, y está siendo actualmente reemplazado de manera gradual por métodos modernos, pero todavía se usa. Para más detalles sobre como funciona un espectrómetro Dobson pincha
|
|
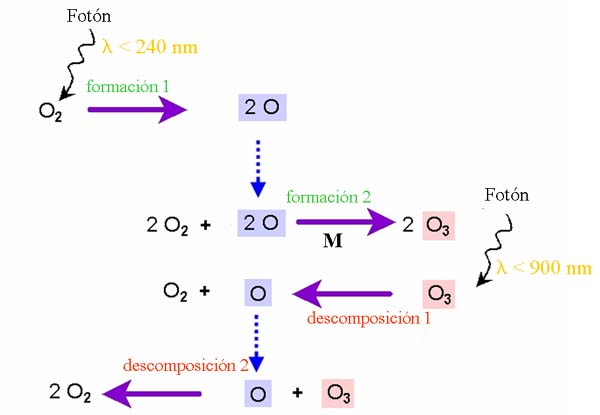
Las reacciones de Chapman
3 O2 -> 2 O3 y 2 O3 -> 3 O2
|
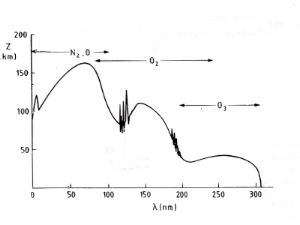
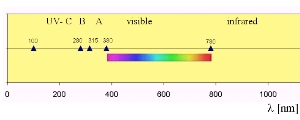
Absorción en el UVDependiendo de la absorción de una molécula, un enlace puede ser roto por la radiación pura. Cada molécula absorbe energía en un rango determinado del espectro electromagnético. El oxígeno absorbe en el rango de alta energía del UV-C, el ozono en el rango UV-B, que es un poco menos energético. Longitudes de onda más larga atraviesan la atmósfera parcialmente y llegan a la superficie de la Tierra. 5. Espectro de absorción ( a la derecha):
|
|
|
Sin embargo, una pequeña fracción de la radiación UV-B alcanza la superficie de la Tierra, permitiendo la formación de radicales OH que limpian la troposfera. Esta fracción es crítica también para las consecuencias biológicas como las quemaduras del sol y el daño del ADN.
|
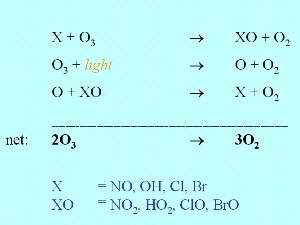
La reducción del ozono por parte de los radicalesPoco a poco se fue demostrando que las concentraciones medidas de ozono no podían explicarse simplemente con las sencillas reacciones de Chapman. Desde 1970 Crutzen, Molina, Rowland (Premio Nobel de 1995) y otros científicos han desarrollado la teoría de una implicación de los óxidos de nitrógeno y de los radicales halógenos en la química del ozono. Molina y Rowland ya habían descubierto en 1974 que los clorofluorocarbonos destruyen el ozono.
|
|
|
Desde que se conoció que las actividades humanas liberan compuestos que contienen halógenos, los científicos pronosticaron un ligero descenso de la concentración de ozono. Sin embargo, la idea de los procesos estratosféricos no era aún conocida totalmente, y hasta que en 1985 se detectó el agujero de la capa de ozono sobre la Antártida, nunca se había esperado una disminución tan drástica de ozono como la sufrida por éste.
|
Sobre esta página:autor: Dr. Elmar Uherek - MPI for Chemistry, Mainz
|