> Español > Climate Encyclopaedia > estratosfera > Más > 2. Ozono > - Química del cloro
> Español > Climate Encyclopaedia > estratosfera > Más > 2. Ozono > - Química del cloro
|
Alta AtmósferaSaber más
|
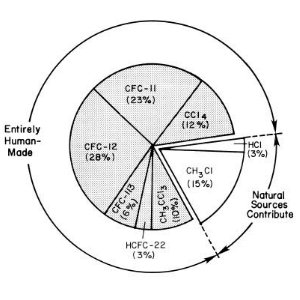
Química del cloroFundamentalmente, la química de cloro está llevando a la destrucción de la capa de ozono. Con la producción industrial de clorofluorocarbonos (CFCs), el hombre introdujo una nueva fuente de cloro en la atmósfera. Ahora, el nivel de cloro es seis veces mayor de lo que era debido a sus fuentes naturales, con unas consecuencias fatales para la capa de ozono. Sin embargo, las condiciones para la formación del agujero de la capa son muy especiales. Por ello, no se había previsto un desarrollo tan drástico.
|
Química del cloro estratosférico
|
|
Pero el radical del inicio X
|
|
ClO
|
|
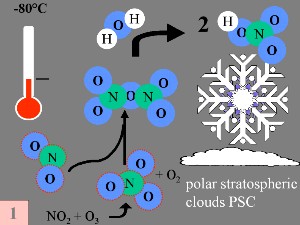
Las condiciones especiales del agujero de la capa de ozono de la AntártidaDurante la noche polar con temperaturas de alrededor de -80°C, la pequeñísima cantidad de agua disponible en la estratosfera es capaz de congelarse y de formar nubes estratosféricas, junto con ácido nítrico (el llamado ácido nítrico trihidratado ANT, o NAT). Ahora las cinco condiciones clave vienen de la mano:
|
|
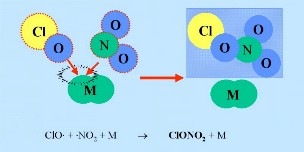
Primera: Los catalizadores del óxido de nitrógeno( óxido de nitrógeno NO y dióxido de nitrógenoNO2), que ayudan a convertir el ClO produciendo por lo tanto ácido nítrico HNO3 que es incorporado a las partículas de las nubes estratosféricas polares (NEP o PSC).
|
|
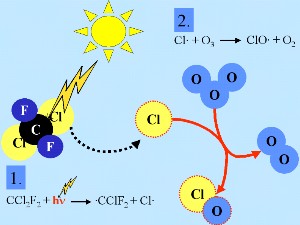
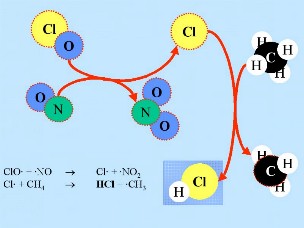
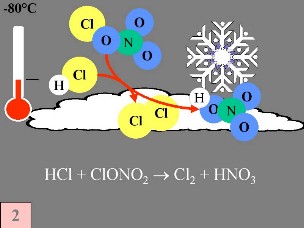
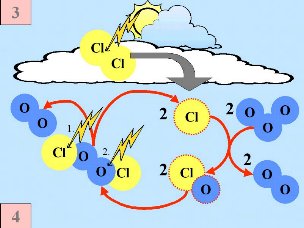
Segunda: En la superficie de las nubes estratosféricas polares (NEP o PSC) las partículas de hielo de las "especies de reserva" de cloro no reactivo, HCl y ClONO2, reaccionan entre sí para producir Cl2 y HNO3; éste último es inmediatamente incorporado a las partículas. Tercera: Cuando vuelve a hacerse de día al final de la noche polar, el Cl2 es fotolizado y produce dos radicales de Cl. El cloro se ha reactivado.
|
|
Cuarta: Los átomos de cloro comienzan una cadena de reacciones catalíticas, conduciendo a la destrucción del ozono siempre y cuando no haya óxidos de nitrógeno disponibles que los eliminen. Hay que tener en cuenta que la relación entre la velocidad de destrucción del ozono y la concentración de cloro ( o ClO) es cuadrática. Cl
|
|
Quinta: Las especies de cloro más habituales como el Cl
|
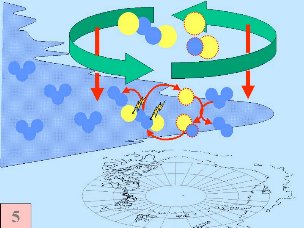
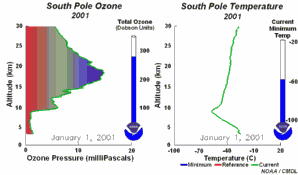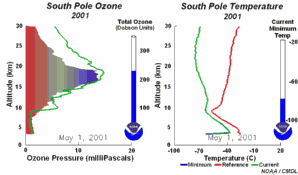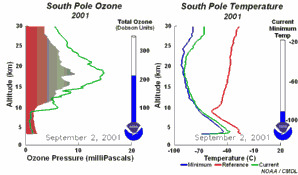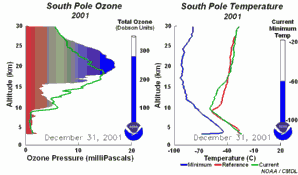
Las cinco condiciones deben darse a la vez para formar el agujero de la capa de ozono. Por esta razón la mayor destrucción de ozono tiene lugar sobre la Antártida y únicamente durante los meses de septiembre / octubre (primavera antártica), en los que el sol sale después de la noche polar. En pocos años, tenemos unas condiciones comparables en el Ártico en Marzo, y también un pequeño agujero se va formando en el Norte de Europa. Al final del año, las nubes polares se disuelven, los óxidos de nitrógeno vuelven a estar disponibles, el vortex polar se quebranta y los radicales de cloro son eliminados; por lo que la capa de ozono se recupera.
|
|
M*: En cualquier tipo de reacción A + B -> C es necesario un tercer compañero, que elimina la energía en exceso. De otro modo el producto C podría tener la misma energía que la suma de los reactivos A + B y directamente se produciría la reacción inversa. En la mayoría de los casos M es el nitrógeno del aire N2.
|
Sobre esta página:autor: Dr. Elmar Uherek - MPI for Chemistry, Mainz
|