> magyar > Climate Encyclopaedia > Felsõ légkör > Haladó > 2. Ózon > - Sztratoszférikus. Ózon
> magyar > Climate Encyclopaedia > Felsõ légkör > Haladó > 2. Ózon > - Sztratoszférikus. Ózon
|
Felsõ légkörHaladó |
A sztratoszférikus ózon kémiájaCsak 1980 után történt, hogy a sztratoszférikus ózon kémiájáról ismereteink rohamosan növekedtek. Ennek az oka az 1985-ös ózonlyuk felfedezése volt. A következõ két részben történeti keretben kitekintést adunk a sztratoszféra kémiájáról.
|
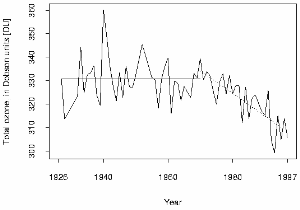
Az ózon felfedezése és az elsõ mérésekAz ózon kutatás meglehetõsen régi területe a légkör tudománynak. 1840-ben a gázt ózonnak (szagos) keresztelte Christian Friedrich Schönbein kémikus, aki felfedezte, hogy ez az anyag képzõdik elektromos kisülésekkor. Nagyon hamar kiderült, hogy az ózon a levegõ természetes része. Ennek a gáznak az elsõ mérési módszerét Schönbein fejlesztette ki, de nagyon hamar ezt továbbfejlesztették Párizsban, a Mt. Souris Obszervatóriumban. Onnantól kezdve származnak az elsõ adatsorok (1876-1910), melyek ma a legjobb becslései az iparosodás elõtti határrétegbeli koncentrációnak.
|
|
|
1879-ben felfedezték, hogy a Nap spektruma jelentõsen lecsökken az UVB tartományban a Földi felszíne közelében, és 1880-ban felfedezték, hogy az ózon egy erõs elnyelõ ebben a tartományban, és az lehet felelõs ezért. Az alsó légkörben megtalálható ózon mennyiség, azonban nem magyarázza meg ezt az UVB csökkenést. Ennek következtében megszületett a feltevés, hogy a legtöbb ózonnak magasabb légrétegekben kell képzõdnie. A kulcsfontosságú kutatást Gordon Dobson végezte el a XX. század 20-as éveiben. Kifejlesztette a Dobson - spektrométert, amit 1929 óta használunk a teljes légoszlop ózon mennyiségének megmérésére, és manapság ugyan fokozatosan helyettesítik sokkal modernebb eljárásokkal, de még mindig használják. Arról, hogy hogyan mûködik a Dobson spektrométer, többet itt találhatsz, kattints
|
|
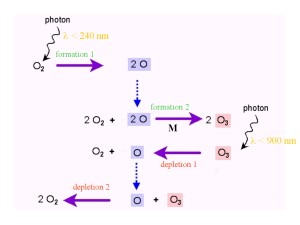
A Chapman reakció
3 O2 -> 2 O3 és 2 O3 -> 3 O2
|
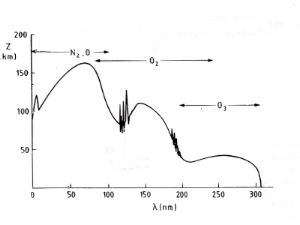
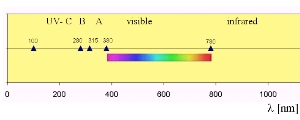
Abszorpció az UV tartománybanA molekula abszorpciójától függ, hogy egy molekulát csak tisztán fénnyel fel tudunk-e bontani. Minden molekula az elektromágneses spektrum bizonyos részének az energiáját elnyeli. Az oxigén abszorbeálja a nagyenergiájú UV-C tartományt, az ózon a valamivel kevésbé energikus UV-B-t. A hosszabb hullámhossztartományok részben áthaladnak a légkörön és elérik a Föld felszínét. 5. Abszorpciós spektrum (jobbra):
|
|
|
Az UV-B egy kis része azonban eléri a földfelszínt, hozzájárulva az OH gyök képzõdéshez, ami tisztítja a troposzférát. Ez a tartomány kritikus a biológiában is, beleértve lebarnulást vagy a DNS károsodását.
|
Gyökök miatti ózoncsökkenésEgyre világosabbá vált, hogy a mért ózonkoncentráció nemcsak az egyszerû Chapman reakciókkal magyarázható. 1970-tõl Crutzen, Molina, Rowland (Nobel díj, 1995) és más tudósok kidolgozták a halogén gyökök és nitrogén-oxidok részvételének elméletét az ózon kémiájában. Molina és Rowland már 1974-ben felfedezték, hogy a halogénezett szénhidrogének rombolják az ózont.
|
|
|
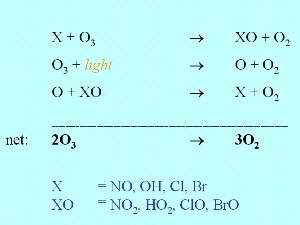
Az ózon nem csak fotolízissel bomlik el, hanem X gyökökkel lezajló reakciójával is, mely lehet nitrogénmonoxid, NO, hidroxilgyök, OH vagy egy halogén gyök mint Cl vagy Br. Van több más olyan, kisebb a fontosságú gyök is, amelyek hasonló módon reagálnak. Mivel a halogént tartalmazó vegyületek kibocsátása emberi tevékenységbõl származik és ismert, csekély ózonkoncentráció csökkenést jósol néhány tudós. Azonban a sztratoszférára vonatkozó folyamatokról szóló ismereteink nem voltak teljesek, és egy ilyen nagymértékû ózoncsökkenést, mint az Antarktisz fölötti ózonlyuk nem vártak, mielõtt 1985-ben felfedezték azt.
|
Az oldalról:szerzõ: Dr. Elmar Uherek - MPI for Chemistry, Mainz
|