> Italiano > Climate Encyclopaedia > Bassa atmosfera > Approfondimento > 4. Gas nell'atmosfera > - Distribuzione & concentrazione (2)
> Italiano > Climate Encyclopaedia > Bassa atmosfera > Approfondimento > 4. Gas nell'atmosfera > - Distribuzione & concentrazione (2)
|
Bassa AtmosferaApprofondimento |
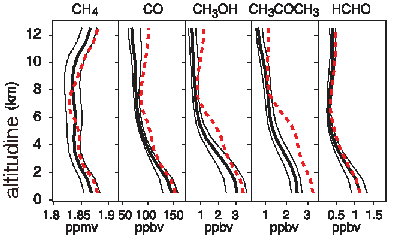
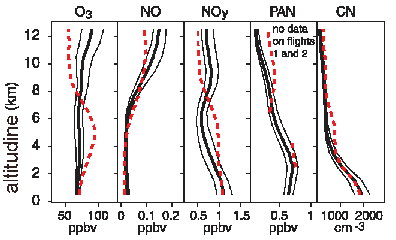
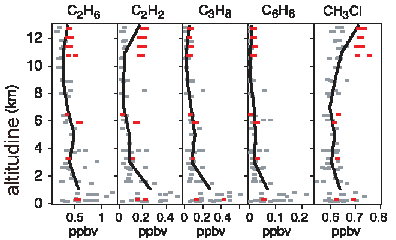
Distribuzione & concentrazione (2)Per i composti atmosferici meno stabili è impossibile dare delle concentrazioni atmosferiche medie. Le loro concentrazioni dipendono fortemente dalla chimica dellatmosfera che si verifica in un momento specifico. |
|
Composti misurati: CH4 = metano
|
|
O3 = ozono
|
|
C2H6 = etano
|
Gas nella troposferaE' molto difficile dare una visione d'insieme delle concentrazioni dei gas in tracce presenti nella troposfera. Lo stesso composto può avere ad esempio concentrazioni molto basse sopra l'oceano e concentrazioni molto alte in ambiente urbano. Inoltre sono moltissimi i gas che svolgono un ruolo importante nella troposfera. Perciò la seguente tabella mostra alcuni esempi dei rapporti di mescolamento medi vicino al suolo di quei composti misurati più comunemente.
|
|
Tabella riassuntiva che riporta i più importanti gas presenti nell'atmosfera libera:
*Le concentrazioni dei gas indicate con un asterisco sono quelle aumentate a causa dell'attività dell'uomo e sono relativamente ben rimescolate a livello globale. I valori percentuali dei componenti principali dell'aria sono dati per l'aria secca. Dati del 2005-2007.
|
Rapporti di mescolamento, concentrazioni a unità di misura diverse:Le quantità di gas possono essere espresse con diverse unità di misura: concentrazione: molecole cm-3 o µmol m-3 Il rapporto di mescolamento è ununità di misura scientificamente più corretta: quando l'aria sale, si espande in volume e, di conseguenza, la concentrazione di gas cambia. Il rapporto di mescolamento (la proporzione relativa sul numero totale di molecole d'aria), tuttavia, rimane lo stesso. La conversione da un'unità di misura all'altra dipende dalla pressione (= l'altitudine) e dal peso molecolare del composto. Se facciamo il calcolo per la superficie della terrestre ad una pressione normale di circa 1 bar possiamo esprimere le molecole totali per volume di aria nei seguenti modi: 1 mol = 22.4 L = 6x1023 molecole => Una stima approssimativa: Perciò il rapporto di mescolamento è circa 2.7 x 1016 / 2.7 x 1025 = 10-9 = 1 ppb Poichè l'ozono ha un peso molecolare simile, M(O3) = 48 g mol-1, possiamo anche dire approssimativamente che; Questo calcolo è valido solo per la superficie terrestre dove viviamo. Per gli episodi di inquinamento da ozono nelle aree urbane possiamo fare questi calcoli: 120 µg m-3 = 60 ppb -> livelli alti
|
|
Pagine collegate Ulteriori informazioni sulle concentrazioni e i rapporti di mescolamento sono disponibili in:
|
A proposito di questa pagina:Versione italiana: Laura Dini (traduttore) e Michela Maione (revisione linguistica)
|