> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 4. Gase in der Atmosphäre > - Verteilung & Konzentration (2)
> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 4. Gase in der Atmosphäre > - Verteilung & Konzentration (2)
|
Untere AtmosphäreMehr .. |
Verteilung & Konzentration (2)Möchten wir etwas über die Konzentrationen von weniger stabilen Verbindungen in der Atmosphäre erfahren, so können wir nicht einfach eine Zahl angeben. Sie hängen stark von der Chemie ab, die sich in der Luft abspielt.
|
|
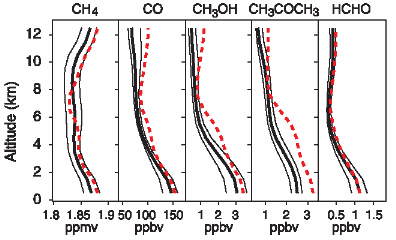
Gemessene Verbindungen: CH4 = Methan
|
|
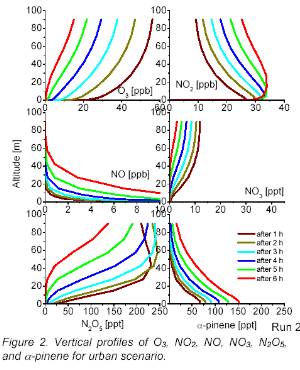
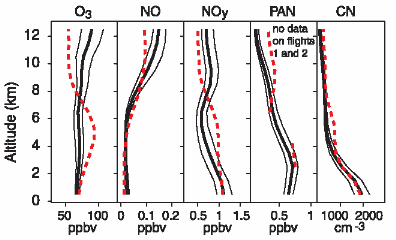
O3 = Ozon
|
|
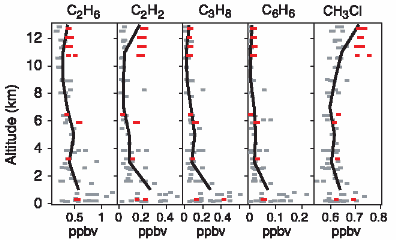
C2H6 = Ethan
|
Gase in der TroposphäreEinen Überblick über die Spurengase in der Troposphäre und ihre Konzentrationen zu geben, ist kaum möglich. Dieselbe Verbindung kann in extrem niedriger Konzentration anwesend sein, z.B. über den Ozeanen, oder in sehr hoher Konzentration, z.B. im städtischen Raum. Auch kann man sicherlich einige Dutzend Gase als wichtig einstufen. Die folgende Tabelle kann daher nur als eine Zusammenstellung von oft gemessenen Verbindungen angesehen werden, für die ein realistisches Mischungsverhältnis (gewöhnlich in Bodennähe) angegeben ist.
|
|
Überblick wichtiger Gase in der freien Atmosphäre:
*Gase, deren Mischungsverhältnis auf Grund menschlichen Eintrags ansteigt, die aber global relativ gut durchmischt sind. Die Angabe der Hauptgase bezieht sich auf trockene Luft. Daten von 2005 - 2007.
|
Mischungsverhältnisse, Konzentrationen und verschiedene Einheiten:Die Menge an Gasen wird oft in verschiedenen Einheiten angegeben: Konzentrationen: Moleküle/cm3 oder µg/m3 Mischungsverhältnisse sind für die Wissenschaftler oft deshalb die günstigere Wahl, weil sich Luft, die aufsteigt, ausdehnt. Das Volumen wächst und damit ändert sich die Konzentration. Das Verhältnis der Gasmengen zueinander jedoch, das Mischungsverhältnis, bleibt im selben Luftpaket gleich. 1 Mol eines Gases enthält 6x1023 Moleküle und nimmt (bei Normbedingungen) das Volumen von 22,4 L ein. Demnach sind enthalten in Beispiel für eine Abschätzung: Damit ist das Mischungsverhältnis in Näherung: 2,7x1016 / 2,7x1025 = 10-9 = 1 ppb Da Ozon eine sehr ähnliche Molmasse hat, nämlich M(O3) = 48 g/mol, können wir auch sagen
|
Verwandte Seiten:Weitere Erklärungen zu Konzentrationen und Mischungsverhältnissen am Beispiel des stratosphärischen Ozons finden sich in
|
About this page:Author: Dr. Elmar Uherek - Max Planck Institute for Chemistry, Mainz
|