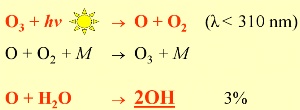> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 1. Oxidation und Beobachtung > - Oxidation & OH
> Deutsch > Climate Encyclopaedia > Untere Atmosphäre > Mehr > 1. Oxidation und Beobachtung > - Oxidation & OH
|
Untere AtmosphäreMehr |
Oxidation in der AtmosphäreViele chemische Verbindungen werden in die Atmosphäre entlassen. Sie würden sich dort ansammeln, gäbe es nicht auch Wege, sie wieder zu entfernen. Dies kann durch trockene Ablagerung (trockene Deposition) oder durch Auswaschen mit dem Regen geschehen. Besonders bei organischen Verbindungen ist das Entfernen einfacher, wenn sie vorher in einen weniger flüchtigen, wasserlöslichen Zustand oxidiert wurden ...
|
|
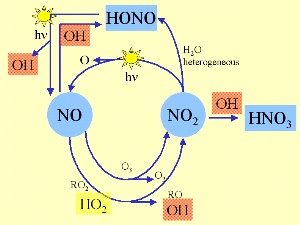
Oxidation im chemischen Sinne muss nicht immer bedeuten, dass eine Reaktion mit Sauerstoff enthaltenden Verbindungen stattfindet. In der Luft allerdings ist Sauerstoff fast immer mit von der Partie. Drei wichtige Oxidationsmittel bestimmen die Prozesse in der Atmosphäre: das Hydroxyl-Radikal OH Auch Hydroperoxy-Radikale HO2 sind wichtig und manchmal fasst man die Summe von OH und HO2 als HOx zusammen. Das wichtigste Oxidationsmittel jedoch ist das OH-Radikal. Es ist sehr reaktiv und in der Lage, die meisten chemischen Verbindungen in der Troposphäre zu oxidieren.
|
|
Wie wird OH gebildet?OH bestimmt die atmosphärische Chemie vor allem während des Tages, denn seine Bildung hängt von der Sonnenstrahlung ab. Die auslösende Reaktion (siehe oben) ist die Spaltung von Ozon durch Sonnenlicht (Photolyse), die Licht einer Wellenlänge von weniger als 310 nm erfordert. Es folgt eine Reaktion des hierbei gebildeten O-Atoms mit Wasser. Aus diesem Grund ist eine geringe Menge an Ozon in der Troposphäre notwendig, auch wenn zu viel schädlich ist.
|
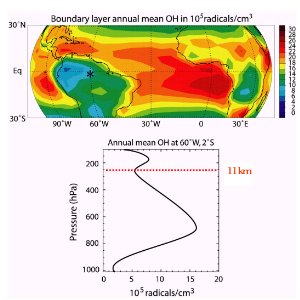
Wieviel OH wird gebildet?Da OH ein extrem reaktives Radikal ist, reagiert es sofort wieder ab, sobald es gebildet wird. Seine Lebensdauer liegt bei einer Sekunde oder weniger. Daher ist die mittlere Konzentration in der Luft sehr gering, im Bereich von 1x105 bis 2x107 Moleküle cm-3. Dies entspricht für den Luftdruck auf Meereshöhe einem Mischungsverhältnis von 0,01 - 1 ppt (pmol/mol). Von 1000 - 100.000 Milliarden Teilchen in der Luft ist nur eines OH.
|
|
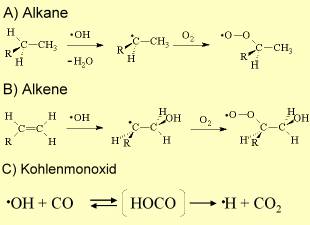
In besonderem Maße nimmt die Konzentration aber auch mit der geographischen Breite ab, nicht nur auf Grund der sinkenden Wasserdampfkonzentration, sondern auch, weil die Intensität des Sonnenlichtes und die Sonnenscheindauer in Richtung der Pole abnehmen. Wie reagiert OH?Das Bild rechts zeigt einen interessanten Effekt über dem tropischen Regenwald. Die OH-Konzentration sinkt in der Nähe des Bodens. Was ist der Grund? Viele organische Verbindungen, vor allem Isopren, werden vom Wald emittiert und reagieren mit OH. Daher wird OH in Bodennähe verstärkt in chemischen Reaktionen verbraucht. OH neigt dazu, wenn immer möglich, die H-Atome von einer organischen Verbindung RH abzuspalten und Wasser H2O zu bilden. Im nächsten Schritt reagiert das Radikal R
|
|
|
Nun reagiert weltweit gesehen OH aber nicht vor allem mit organischen Verbindungen aus Wäldern. Größere organische Verbindungen tragen nur zu etwa 30% zum OH Abbau bei, weitere 15% alleine das Methan, das wichtigste und kleinste organische Molekül. Das Gas, was jedoch hauptsächlich mit OH reagiert, ist Kohlenmonoxid (40% Anteil). Die verbleibenden 15% tragen Ozon O3, Hydroperoxy-Radikale HO2 und Wasserstoff H2 bei. |
|
In der Reaktion mit kleinen Alkenen neigt OH dazu, sich an die Doppelbindung anzulagern, solange der gesättigte Rest nicht viel größer ist und die Abspaltung eines H-Atoms statistisch begünstigt ist. Auch in der Alkenreaktion werden Peroxide gebildet.
|
Wenngleich OH das wichtigste Oxidationsmittel in der Atmosphäre ist, sind die Konzentrationen nachts nahezu null, da die Bildung Sonnenstrahlung erfordert. Darum wird in der Dunkelheit der Nacht die Chemie von Nitrat-Radikalen NO3 und auch Ozon O3 wichtiger.
|
|
|