|
|
 |
|
|
|
 |
| |
|
|
 |
Untere Atmosphäre
Basis |
Emissionen* der Biosphäre
Es werden nicht nur Treibhausgase in die Atmosphäre emittiert, sondern tausende anderer chemischer Verbindungen. Viele von ihnen sind organische Verbindungen. Die Pflanzenwelt (Bäume, Plankton im Ozean und andere Pflanzen) emittiert weltweit gesehen weit mehr von ihnen, als wir Menschen.
|
|
|
|
|
 |
|
Kohlenstoff ist ein wichtiges Element in der lebendigen Welt. Chemische Verbindungen, die vor allem aus Kohlenstoff und Wasserstoff und manchmal noch einigen anderen Elementen (Sauerstoff, Stickstoff, Phosphor, Schwefel) bestehen, werden organische Verbindungen oder Organika genannt. Wir Menschen emittieren eine Menge solcher organischen Verbindungen in Lösemitteln, Autoabgasen und vielen chemischen Industrien, z.B. Raffinerien. Da die meisten von uns in Städten wohnen, ist es schwer zu glauben, dass wir nicht die Hauptproduzenten sind. Aber weltweit gesehen gibt es immer noch riesige kaum besiedelte Waldregionen und Savannen und natürlich die Ozeane, in denen die natürlichen Emissionen dominieren.
|
 |
 |
|
1. Reisfeld - Bali, Indonesien
Quelle: STRINGER/INDONESIA für Reuters
|
|
 |
Was emittieren Pflanzen?
Gehen wir durch einen Wald oder durch Grasland, so bekommen wir einen Eindruck vom Geruch verschiedenster organischer Gase, die von den Bäumen, dem Gras und den Blumen freigesetzt werden. Weltweit werden jedes Jahr mehr als 1000 Millionen Tonnen solcher Organika emittiert. Hierzu zählt eine gewaltige Menge der organischen Substanzen Isopren (mehr als 500 Mio Tonnen pro Jahr) und Monoterpene (130 Mio t/Jahr). Rieche an den Nadeln einer Pinie oder eines anderen Nadelbaumes und ein solches Monoterpen dringt in deine Nase.
|
Pflanzen bilden solche Stoffe und setzen sie durch Blätter und Nadeln frei. Sie tun dies ganz besonders in Reaktion auf Trockenheit, Hitze und Stress, aber auch während ihres normalen Lebenszyklus. Auch werden jedes Jahr etwa 200 Mio t an Methangas aus natürlichen Quellen freigesetzt. Hier jedoch trägt der Mensch etwa nochmal dieselbe Menge vor allem aus Viehhaltung und Reisfeldern bei.
Wir müssen daran denken, dass 71% der Erde von Wasser bedeckt sind und auch die Ozeane sind lebendig und enthalten z.B. große Mengen an Phytoplankton (Algen). Die Chemie in diesen Pflanzen liefert pro Jahr ca. 45 Mio Tonnen Dimethylsulfid (DMS) an die Atmosphäre. Dieses sogenannte schwefelorganische Gas wird in der Luft zu Schwefelsäure oxidiert und führt zur Bildung von Wolken über den Ozeanen.
|
 |
 |
 |
|
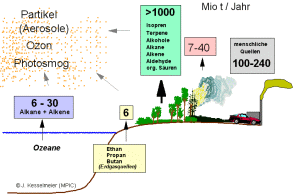
1.a) Weltweite Emissionen von gasförmigen organischen Verbindungen in Mio Tonnen pro Jahr (Methan und DMS nicht eingeschlossen). Die Verbindungen werden von den Ozeanen, aus dem Boden, in großen Mengen von Pflanzen, von Feuern und aus menschlichen Quellen emittiert.
Bild: Jürgen Kesselmeier
Bitte das Bild zum Vergrößern anklicken! (30 kB)
|
|
 |
 |
|
|
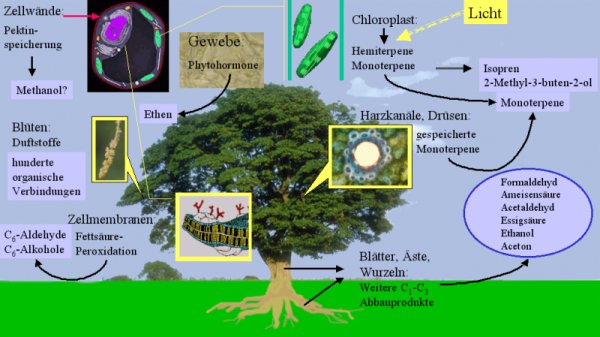
2. Der Baum als Produktionsort für organische Verbindungen (nach N.C. Hewitt; Bild: Elmar Uherek)
Isopren (ca. 500 Mio t/Jahr weltweit) und Monoterpene (ca. 130 t/Jahr) sind wichtige organische Verbindungen, die in großen Mengen von Bäumen und anderen Pflanzen in die Atmosphäre entlassen werden. Aber es gibt noch viele andere Stoffe, die Pflanzen erzeugen.
Bild bitte zum Vergrößern anklicken! (100 kB)
Hochaufgelöstes Bild (500 kB) -> HIER KLICKEN
Das Klimasystem im Ganzen zu verstehen, bedeutet also nicht nur zu beobachten, wie sich die Emissionen aus menschlichen Quellen ändern. Es bedeutet auch zu verstehen, wie Pflanzen zu den weltweiten Kreisläufen beitragen und welche Veränderungen hier vorgehen. Betrachten wir drei Beispiele näher.
|
 |
 |
|
3. Der bläuliche Dunst, der den Great Smooky Mountains (USA) ihren Namen gab, ist wohl auf die Bildung von biogenen Partikeln zurückzuführen.
|
|
 |
Bsp. 1: Monoterpene
Monoterpene bestimmen den Duft des Waldes und auch den Geruch mancher Früchte. Es handelt sich um ungesättigte Verbindungen, die aus Kohlenstoff, Wasserstoff und manchmal Sauerstoffatomen bestehen. Sie haben wohlklingende Namen wie Limonen oder Pinen [Betonung auf der letzten Silbe]. Poduziert werden sie von Bäumen und anderen Pflanzen, ganz besonders mit dem ersten Sonnenlicht an warmen Tagen. Die Substanzen können gespeichert oder direkt in die Atmosphäre entlassen werden. Stehen Pflanzen unter Stress, so erhöhen sie die Produktion.
|
|
|
 |
4. Im Bild links siehst Du die chemische Struktur eines Monoterpens, beta-Pinen (links) und die einer der wichtigsten natürlichen organischen Verbindungen überhaupt, Isopren (rechts). Beide Verbindungen sind ungesättigt. Dies bedeutet, sie haben eine C=C Doppelbindung. Sie ist durch den roten Kringel hervorgehoben. Um Arbeit beim Zeichnen komplizierter organischer Verbindungen zu sparen, geben Chemiker meist die C- und H-Atome nicht an. Isopren ist in beiden Formen dargestellt. Einmal mit C und H Atomen (unten), einmal ohne (darüber).
|
Pflanzenemissionen reagieren in der Atmosphäre
Einmal in die Atmosphäre emittiert, werden Terpene durch OH Radikale oder Ozon oxidiert. In der Luft laufen viele chemische Reaktionen ab. Die Produkte sind Substanzen, die in der Luft kondensieren können. Sie können sich entweder an der Oberfläche von Pflanzen oder dem Boden absetzen, sie können aber auch in der Luft zu Partikeln zusammenwachsen. Solche in der Atmosphäre schwebenden Partikel nennen wir Aerosol. Sie sind wichtig, um Wolken zu bilden. So können verschiedene Substanzen in den Partikeln auch zur Bildung verschiedener Wolken führen. Pflanzenemissionen wie Abgase aus menschlichen Quellen beeinflussen also die Wolkenbildung. Die Bildung von Aerosolen kann sogar für unser Auge sichtbar sein. Ein Beispiel ist der blaue Dunst über den Wäldern (Bild 3). Mit Piniennadeln und Ozon können wir die Partikelbildung auch im Versuch nachvollziehen (Bild 5).
|
 |
 |
 |
|
5. Versuch zur Bildung von blauem Dunst im Labor (durchgeführt am MPI Mainz).
Der Strahl einer starken Lampe hilft den Dunst sichtbar zu machen, der sich in dem Plexiglaskasten bildet, sobald Ozon aus der einen Hälfte der Box mit Monoterpenen aus den Piniennadeln in der anderen Hälfte in Kontakt kommt.
Foto: Elmar Uherek
Bitte zum Vergrößern anklicken (60 K)
|
|
 |
 |
|
6. Medicago varia (Fabaceae)
Luzerne und andere Lippenblütler werden in der Landwirtschaft zur Stickstoffbindung genutzt.
Photo: Patrick Knopf, spez. Botanik, Ruhr-Universität Bochum
|
|
 |
Bsp. 2: Distickstoffmonoxid N2O - Lachgas
Stickstoff ist ein wichtiges Element in der Biosphäre und Bestandteil z.B. von Proteinen, Aminosäuren, der DNA oder Energie übertragenden Molekülen. Pflanzen nehmen den Stickstoff aus dem Ammoniak im Boden auf. Bakterien helfen, ihn in dieser Form verfügbar zu machen, indem sie Stickstofffixierung, d.h. Aufnahme von Stickstoff aus der Luft, betreiben. Bakterien bauen aber auch wieder die Nitrate ab und wandeln sie in Distickstoffmonoxid (Lachgas) um, welches in die Luft entweicht. Da Distickstoffmonoxid N2O eine sehr stabile Verbindung ist, die in der Troposphäre kaum abgebaut wird, wird sie zur wichtigsten Stickoxidquelle für die Stratosphäre. Dort nimmt sie an Reaktionen teil, die Ozon abbauen. Der Stickstoff kommt schließlich als Salpetersäure (HNO3) wieder zurück zur Erde. Die Stickoxidemissionen sind relativ stark angestiegen aufgrund von verstärkter Düngung in der Landwirtschaft. Etwa 15 Mio Tonnen pro Jahr werden weltweit emittiert.
|
Bsp. 3: Dimethylsulfid
Kleine unsichtbare Partikel von Schwefelsäure und Wasser ermöglichen die Wolkenbildung über den Ozeanen. Aber woher kommt die Schwefelsäure? Schwefelverbindungen sind von hoher Bedeutung im Stoffwechsel der marinen Pflanzenwelt, da Schwefel überall in den Ozeanen verfügbar ist. Algen (Phytoplankton) z.B. benötigen besondere Schwefelverbindungen zur Regulation ihres Wasserhaushaltes. Durch ihren Abbau entsteht die schwefelorganische Verbindung Dimethylsulfid, ein Gas, das in die Luft entlassen wird. Dort erfolgt die Oxidation erst zu Schwefeldioxid, dann zu Schwefelsäure. Diese wiederum ist wichtig für die Wolkenbildung.
Die Einheit 3 im Basiskapitel des Themas ‚Ozeane' erklärt die besondere Rolle von Phytoplankton in den Meeren näher.
|
 |
 |
 |
|
7. Die Veranschaulichung des Chlorophylls in Phytoplankton
Das Satellitenbild zeigt den Atlantischen Ozean an der Ostküste Kanadas. Es ist jedoch nicht nur Wasser in der See. Die Animation schaltet zu einem Bild, das das Phytoplankton im Ozean (steigende Konzentration von blau nach rot) sichtbar macht. Dieses emittiert große Mengen Dimethylsulfid in die Luft.
Quelle: SEAWIFS Projekt
|
|
|
Diese wenigen Beispiele geben einen Eindruck davon, in welch komplexer und enger Weise die Emissionen der Pflanzenwelt mit dem Klima verknüpft sind.
* Unter Emissionen (Verb: emittieren, lat.: emittere = aussenden, herauslassen) verstehen wir in der Klimakunde die Abgabe oder Aussendung von Chemikalien (Schadstoffe, natürliche Stoffe aus Pflanzen, Abgase) in die Umwelt.
|
Verwandte Seiten:
Die Rolle von Schwefelgasen aus Phytoplankton ist erklärt in
Ozeane - Basis - Einheit 3 - Schwefelgase
Artikel zur ozeanischen Nahrungskette und der Rolle der Schwefelverbindungen im
ACCENT Global Change Magazin - Ausgabe Nr. 5 - Januar 2005
About this page:
author: Dr. Elmar Uherek - MPI for chemistry, Mainz
educational proofreading: Michael Seesing - Uni Duisburg - 2003-07-02
1. scientific reviewing: Prof. Jürgen Kesselmeier - MPI for chemistry, Mainz - 2003-07-15
2. scientific reviewing: Dr. Pascal Guyon - MPI for chemistry, Mainz - 2004-05-10
Letzte Überarbeitung: 2007-08-20
|
|
 |
|







