|
|
 |
|
|
|
 |
| |
|
|
 |
Die Ozeane
Basis |
Andere wichtige Klimagase aus Seewasser - 1
Eine ganze Reihe verschiedener Gase aus dem Seewasser werden in die Atmosphäre entlassen und viele davon nehmen auch Einfluss auf unser Klima. Einige, wie das Dimethylsulfid, werden beim Wachstum von Phytoplankton produziert. Andere entstehen, wenn das Sonnenlicht mit organischen Substanzen in den Oberflächenschichten der Ozeane reagiert. Viele dieser organischen Substanzen kamen ursprünglich auch aus dem Phytoplankton. Wir schauen uns einige dieser Gase, die mit der Luft in der Troposphäre, der untersten Schicht der Atmosphäre, in Kontakt kommen, näher an.
|
|
|
|
|
 |
Halogenkohlenwasserstoffe
Halogenkohlenwasserstoffe sind eine Gruppe einfacher organischer Verbindungen (organisch = auf Kohlenstoff basierend), die Halogenatome enthalten. Halogene ist der zusammenfassende Name für die 7. Hauptgruppe des Periodensystems der Elemente, die Fluor, Chlor, Brom und Iod enthält. Während Fluor im Klimasystem kaum Bedeutung hat, sind die anderen Halogene sehr wichtige Elemente im Seewasser und in der Atmosphäre. Das Wort halin', das Salz oder Salzgehalt bedeutet, ist mit dem Wort Halogen verwandt. Chlor in der Form seines Anions Chlorid (Cl-) ist die wichtigste chemische Spezies im Seewasser, abgesehen vom Wassermolekül selbst.
Eine der bedeutendsten Verbindungen, die zu den Halogenkohlenwasserstoffen gehört, ist Methyliodid mit der chemischen Formel CH3I.
Woher kommen marine Halogenkohlenwasserstoffe?
|
 |
 |
|
1. Makroalgen
Bild: NOAA
|
|
 |
Halogenkohlenwasserstoffe werden durch biologische Prozesse und Sonnenlicht in Seewasser erzeugt. Methyliodid wird von einigen Makroalgen und Phytoplankton-Arten produziert. Es ist nicht genau bekannt, zu welchem Zweck diese Produktion erfolgt. Es ist auch belegt, dass Methyliodid durch die Einwirkung auf iodorganische Verbindungen im offenen Ozean freigesetzt wird. Dies ist wahrscheinlich die Hauptquelle. Ein kleiner Teil der im Meer produzierten Verbindung entweicht auch in die Atmosphäre.
|
Welche Bedeutung haben Halogenkohlenwasserstoffe?
Viele iod- und bromhaltigen Halogenkohlenwasserstoffe können in der Troposphäre (untere Atmosphäre) von Sonnenlicht zerstört werden. Sie bilden reaktive Halogenradikale. Hierin unterscheiden sie sich von Fluorchlorkohlenwasserstoffen (FCKW). FCKW werden nämlich erst durch das energiereichere UV-Licht in der Stratosphäre (obere Atmosphäre) zerstört.
Halogenradikale sind sehr reaktiv. Ihre größte Bedeutung haben sie in der Zerstörung von Ozon (O3). In der Troposphäre wirkt sich Ozon schädlich auf die menschliche Gesundheit aus und ist auch ein sehr starkes Treibhausgas, das für etwa 15% des zusätzlichen Treibhauseffektes verantwortlich ist. Daher kann die Emission von Halogenkohlenwasserstoffen die troposphärische Ozonkonzentration verringern und die globale Erwärmung vermindern. Andererseits führt eine Reduktion der Menge an Ozon auch zu einer Reduktion der Konzentration an Hydroxyl-Radikalen (OH) in der Troposphäre. Da diese die Luft von schädlichen Chemikalien reinigen, können sich sehr geringe OH-Konzentrationen nachteilig auf die Luftqualität auswirken.
|
 |
 |
|
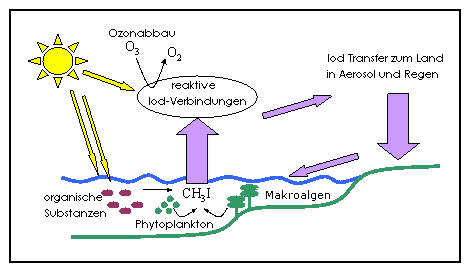
2. Die Zeichnung des marinen Iodzyklus zeigt die wichtigen Quellen von Methyliodid im Seewasser, den Transfer des Iods in die Luft und die Rolle von Iod beim Abbau von Ozon. Sie zeigt auch den bedeutenden Transport von Iod aus dem Ozean auf das Festland, der Gesundheitsprobleme zu vermeiden hilft.
Bild: Lucinda Spokes, nach einer Idee von Dr. Alex Baker, University of East Anglia, Norwich.
|
|
Ein wichtiger Teil des weltweiten Iodkreislaufes ist der Transport von Iod aus den Ozeanen an Land. Diese Iodquelle ist ein kritischer Faktor für die menschliche Gesundheit. Fände ein solcher Transfer nicht statt, so würden die Menschen in weit stärkerem Maße an Hirnschäden und dem Kropf leiden, der die Schilddrüse anschwellen lässt.
|
Methane (CH4)
Methan ist die Hauptkomponente von Erdgas. Es ist ein bedeutendes Treibhausgas und hat sowohl natürliche Quellen als auch solche aus menschlicher Aktivität. Reisfelder und intensive Tierhaltung sind die größten Methanquellen. Aber auch der Ozean ist eine kleine, natürliche Quelle dieses Gases.
Was ist die Quelle von Methan aus dem Ozean?
|
Geht die Sauerstoffkonzentration im Wasser oder in Sedimenten gegen null, dann produzieren Bakterien Methan, wenn sie organisches Material verwerten. Meeresarme, Salzsümpfe und Küstengewässer sind für etwa 75% der gesamten ozeanischen Methanemissionen verantwortlich.
Methan kann auch durch den Einfluss von Wärme und Druck auf verdecktes organisches Material erzeugt werden. Es sind riesige Mengen (größer als die Vorräte aller anderen fossilen Brennstoffe) an sogenanntem Methanhydrat in den Ozeansedimenten gespeichert, die wir zur Versorgung mit Erdgas nutzen könnten. Das meiste Methan, das auf natürlichem Wege aus dem Ozeanboden freigesetzt wird, wird von Bakterien verbraucht, bevor es die Luft erreicht.
|
 |
 |
 |
|
3. Salzsümpfe sind eine wichtige Methanquelle.
Bildquelle: NOAA.
|
|
Wieso ist Methan wichtig?
In der Troposphäre ist Methan ein sehr wirksames Treibhausgas. Es ist 62 mal aktiver als Kohlendioxid (IPCC 2001), bezogen auf einen Zeitraum von 20 Jahren und trägt daher deutlich zur Erderwärmung bei. Es wird angenommen, dass es für 15-20% des zusätzlichen Treibhauseffektes verantwortlich ist. Außerdem kontrolliert es die Konzentration der Hydroxyl-Radikale OH in der Luft. Wenn die Konzentration an Methan steigt, reduziert sich die von OH. Dadurch wird die Möglichkeit der Atmosphäre zur Selbstreinigung eingeschränkt.
Ein Ergebnis der Eutrophierung ist der geringere Sauerstoffgehalt im Wasser. Bleibt die Überdüngung der Küstengewässer auch in Zukunft ein Problem, so wird mehr Methan aus den Ozeanen in die Atmosphäre entlassen.
Ein mögliches Ergebnis der globalen Erwärmung könnte ein Anstieg von Methanemissionen aus den Ozeansedimenten sein, falls das dort vorhandene Methanhydrat (eine Art eisförmiges Methan) teilweise freigesetzt werden sollte. In der jüngeren Erdgeschichte war dies über den Wechsel der Eis- und Warmzeiten hinweg bislang nicht der Fall. Sollte es dazu kommen, so sind wir derzeit nicht sicher, ob die Bakterien das freigesetzte Mehr an Methan noch verarbeiten können. Gelangt es in die Luft, könnte es den Treibhauseffekt deutlich verstärken. Generell wird die Bedeutung der Weltmeere als Methanquelle möglicherweise in Zukunft wachsen.
|
Nicht-Methan Kohlenwasserstoffe (NMHC / NMKW)
Kohlenwasserstoffe (engl.: hydrocarbons HC) sind eine Gruppe von organischen Chemikalien, die nur aus Kohlenstoff und Wasserstoff bestehen. Sie werden in großen Mengen als Kraft- und Brennstoffe eingesetzt (u.a. Erdöl). Der kleinste Kohlenwasserstoff ist das oben bereits diskutierte Methan. Aber auch andere Kohlenwasserstoffe sind bedeutend für das Klima. Der Ozean ist allerdings nur eine kleine Quelle für solche NMHC im Vergleich zu den Quellen auf dem Festland. Auch hier gibt es natürliche und menschliche Quellen. Pflanzen, Böden und fossile Brennstoffe gehören dazu.
Woher kommen NMHC?
|
 |
 |
|
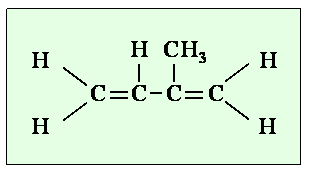
4. Die chemische Struktur von Isopren.
Bild: Lucinda Spokes.
|
|
 |
Im Seewasser werden Nicht-Methan Kohlenwasserstoffe biologisch erzeugt durch die Einwirkung von Sonnenlicht auf organisches Material. Einer der wichtigsten NMHC ist Isopren (2-Methyl-buta-1,3-dien H2C=C(CH3)CH=CH2). Isopren wird sowohl von Landpflanzen produziert als auch von allen Phytoplankton-Arten, die bislang untersucht worden sind. Es ist nicht ganz geklärt, wieso Isopren produziert wird. Möglicherweise handelt es sich nur um ein Nebenprodukt der Photosynthese.
|
Welche Bedeutung haben NMHC's?
Sind NMHC einmal in die Luft entlassen, so reagieren viele von ihnen bereitwillig mit den Oxidationsmitteln in der Luft, tagsüber vor allem mit dem Hydroxyl-Radikal OH, teilweise auch Ozon, in der Nacht mit dem Nitrat-Radikal NO3. In verschmutzter Luft tragen sie zur Bildung von Ozon bei. In reiner Luft, wie wir sie über den Ozeanen finden, bauen sie Ozon ab. Durch ihre Reaktion mit dem Hydroxyl-Radikal OH nehmen sie Einfluss auf dessen Konzentration und seine Fähigkeit, die Atmosphäre von anderen Schadstoffen zu reinigen.
About this page:
author: Lucinda Spokes - Environmental Sciences, University of East Anglia, Norwich - U.K.
1. sci. reviewer: Dr. Bill Sturges, Environmental Sciences, University of East Anglia, Norwich - U.K.
translation: Elmar Uherek, MPI for Chemistry, Mainz 2004-06-28
Letzte Aktualisierung: 2007-09-09
|
|
 |
|







