|
|
 |
|
|
|
 |
| |
|
|
 |
Alsó légkör
Alap |
Troposzférikus ózon
Az ózon valószínûleg a leghíresebb gáz az éghajlattudományban. Miért?
Nagyon ellentmondásos gáz, néha szükséges, néha nem. Egyes emberek panaszkodnak az ózon szmog miatt. A legrosszabb esetben nem közlekedhetsz autóval, mert túl sok ózon képzõdne. |
|
|
|
|
 |
|
Másrészt az emberek panaszkodnak, mert az ózonréteg vékonyabbá válik, és az ózon szükséges, hogy megvédjen minket a bõrráktól. Végül még a tudósok azt mondják, hogy az ózon üvegházgáz, és hozzájárul a Föld felmelegedéséhez. Mi igaz mindebbõl???
Valójában mindegyik igaz.
Látni fogjuk, hogy a talajközeli ózon mennyire káros a növények és az emberek számára, valamint azt, hogy üvegházgáz. A 'Magas légkör' témakörben olvashatsz az ózon mint UV sugárzás elleni védõburok szerepérõl. Látni fogjuk, hogy ugyanannak a gáznak számos hatása lehet.
|
1. a-e) Tartós kár, tipikus példa az ózon levelekre való negatív hatására. Itt: Madárcseresznye Prunus serotina (õszi cseresznye) 0%, 4,4%, 7,8%, 12,3% és 24,5% károsodott.
Forrás: Innes, Skelly, Schaub - Ozon, Laubholz- und Krautpflanzen, ISBN 3-258-06384-2, Copyright by Haupt Verlag AG / Switzerland
Kattints a képekre a nagyításhoz! (körülbelül 25 KB)
|
Az ózon különbözõ tulajdonságokkal rendelkezõ gáz,. Némelyik hasznos, némelyik nem. Ózon a légkör különbözõ szintjeiben elõfordul: Az ózonréteg a sztratoszférában található. Magas ózonkoncentrációt a 25 és 40 km-es magasság között találunk. Ott az ózon hasznos, és megvéd bennünket a bõrráktól. De ebben a fejezetben a troposzféráról beszélünk. Egy kis mennyiségû ózon szükséges a troposzférában, azért hogy a tisztító kémiai folyamatok elinduljanak, de nem túl sok. Az elmúlt évtized alatt, az ózon koncentrációja folyamatosan növekedett a troposzférában. Az átlagos koncentráció növekedett és néha, az ózon szmog alatt, bizonyos területeken olyan magas volt, hogy már veszélyes volt az egészségünkre.
|
 |
 |
 |
|
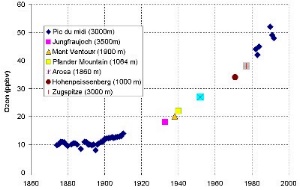
2. Az 1870-es elsõ mérések óta a troposzférikus ózon mennyisége folyamatosan növekszik. A diagram az ózonszintet az összlevegõ százalékában mutatja, 1 milliárd légrész közül mennyi az ózon mennyisége (darab egy milliárdból = ppbv).
Összeállította: Valérie Gros, MPI Mainz, átvéve:
Marenco és mtsai., 1992 (Az ózon hosszúidejû alakulása az Északi félgömb közepes szélességein, Európai Geofizikai Társaság, XVII. gyûlése, 1992. április 6-10, Edinburgh).
|
|
|
|
 |
Veszélyes a légzõrendszerre
Az ózon egy reagens és ingerlõ hatású gáz, ami magas koncentrációban légzési problémákat okoz. Gyulladást okozhat a tüdõben és a hörgõkben, ami általában gyógyítható. A testünk próbálja megvédeni a tüdõnkben lévõ léghólyagokat az ózontól. De ha kevesebb ózon juthat be, akkor az oxigénbõl is kevesebb kerül be
ha az oxigén ellátottság alacsonnyá válik, a szívnek egyre jobban kell dolgoznia. Egyes emberek, akiknek már más egészségi problémái is vannak (például asztma) veszélyben vannak. A legrosszabb esetben az ózon halálhoz vezethet.
|
Az oxigén formái
Az ózon az oxigén speciális formája. A normál oxigén (O2) kettõ oxigén atomot tartalmaz, az ózon hármat (O3). Kevésbé stabil és reaktívabb, mondhatjuk úgy is hogy agresszív. Az ózon képes arra, hogy bontsa a szerves anyagokat, ahogyan a 'Haladó - 3. fejezetében' magyarázzuk. Ez az oka, amiért az emberi szervezetet és a növényzetet is megtámadja, ahogyan a levelek esetében az 1. Ábra mutatja.
|
 |
 |
 |
|
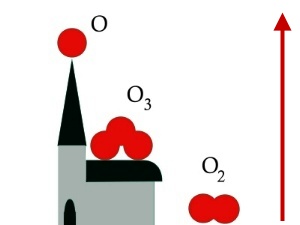
3. Az oxigén három formája, teljesen más a stabilitással. A nyíl a növekvõ reakcióképességet mutatja.
|
|
|
Táblázat: a levegõben lévõ oxigén formái
|
Oxigén formái |
Atomok száma |
Kémiai stabilitás |
Megjelenése a légkörben |
|
Atomos oxigén |
1 atom |
instabil / nagyon reaktív |
elhanyagolható mennyiségben, nyomgáz |
|
'normál' oxigén |
2 atom |
stabil |
a levegõ 21%-a |
|
ózon |
3 atom |
meglehetõsen stabil / reaktív |
10 - 100 ppb | |
ppb = egy darab egy milliárd között
|
Üvegházgáz
Végül, mint a széndioxid (CO2) és a metán (CH4), az ózon is elnyeli a Föld felõl érkezõ hosszúhullámú sugárzást, és hozzájárul az üvegházhatáshoz. A harmadik legfontosabb üvegházgáz. A sugárzási kényszer megnövekedése, 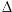 F , az iparosodás óta (körülbelül 1750) a Föld felmelegedéséhez való emberi hozzájárulás mérõszáma. Az ábra a troposzférikus ózon hatását mutatja, összehasonlítva más üvegházgázokkal. F , az iparosodás óta (körülbelül 1750) a Föld felmelegedéséhez való emberi hozzájárulás mérõszáma. Az ábra a troposzférikus ózon hatását mutatja, összehasonlítva más üvegházgázokkal.
Mindezen okok miatt nem akarunk magas ózonkoncentrációt a troposzférában.
|
 |
|
|
Számítsuk ki, hogy melyik gáz mennyivel járul hozzá a globális felmelegedéshez!
A fenti ábra néhány üvegházgáz sugárzási kényszerhez való pozitív hozzájárulását mutatja.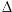 F a tropopauzánál Wm-2-ben van megadva. Az IPCC jelentés (TAR 1. kötet 6.2.1 fejezete) megadja a változó földfelszíni átlaghõmérséklet F a tropopauzánál Wm-2-ben van megadva. Az IPCC jelentés (TAR 1. kötet 6.2.1 fejezete) megadja a változó földfelszíni átlaghõmérséklet 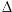 TS és a sugárzási kényszer kapcsolatát. A kapcsolat nagyjából a következõ: TS és a sugárzási kényszer kapcsolatát. A kapcsolat nagyjából a következõ:
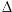 TS / TS / 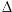 F = 0,5 °C / Wm-2 F = 0,5 °C / Wm-2
Ki tudod számolni a széndioxid, metán, ózon és a nitrogén oxidok által okozott hõmérsékletváltozást?
|
Az oldalról:
szerzõ: Dr. Elmar Uherek - Max Planck Institute for Chemistry, Mainz
tudományos lektor: Dr. Rolf von Kuhlmann, MPI for Chemistry, Mainz
pedagógiai lektor: Michael Seesing - Duisburgi Egyetem - 2003-07-02
utolsó javítás: 2004-04-30
|
|
 |
|







