|
|
 |
|
|
|
 |
 |
|
|
 |
Контекст: круговорот азота
|
Ключевые слова:
фиксация азота, нитрификация, денитрификация, ассимиляция, внесение удобрений, эмиссия оксида азота | |
|
 Круговорот азота Круговорот азота
Круговорот азота необходим для жизни на планете Земля и, конечно, для нас, людей. Соединения азота играют важную роль в обмене веществ живых организмов. Много органических молекул в организме растений, животных и людей включают соединения азота (например, аминокислоты, протеины и ДНК). Соединения азота также участвуют в химических процессах в атмосфере и воздействуют на систему климата.
|
 |
 |
|
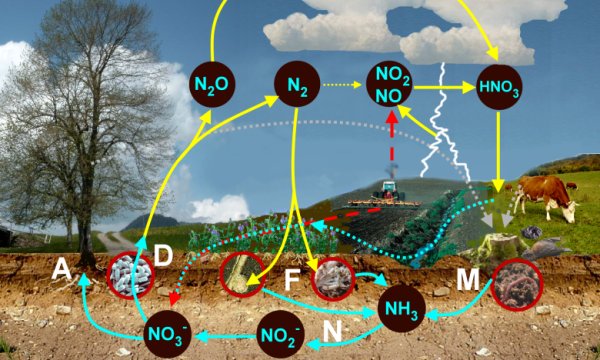
1. Круговорот азота: А – ассимиляция растениями, F – фиксация азота бактериями в симбиозе с растениями или бактериями, живущими в почве, N – нитрификация, D – денитрификация, М – минерализация. Щелкните для увеличения. (140 KB)
Схема: Elmar Uherek
В основном, круговорот азота состоит из химических реакций в воздухе (окисление является доминирующим) и из химических реакций в биосфере: в растениях и микроорганизмах в почве (окисление или востановление).
|
 Фиксация, нитрификация и денитрификация азота Фиксация, нитрификация и денитрификация азота
Для роста растениям необходимы соединения азота. В природе азот может быть в формах, усвояемых растениями (таких как нитраты или соединения аммония) или неусвояемых ими (таких как молекулярный азот или оксид азота). В течение фиксации азота или его денитрификации происходит обмен между обеими формами.
Фиксация азота – процесс усвоения растениями соединений азота из воздуха (главным образом из молекулярного азота, N2). Фиксация азота возможна многими бактериями и цианобактериями. Они живут или в почве, или в симбиозе с растениями, или с несколькими разновидностями животных. Например, семья бобовых растений (Fabaceae) содержит такие бактерии на своих корнях.
Продукты фиксации азота – аммиак, нитриты или нитраты.
Нитрификация является вторым шагом фиксации азота. Если аммиак – первичный продукт фиксации азота, мы можем назвать переход аммиака в нитриты и нитраты (нитрифицирующими бактериями) – нитрификацией.
|
 |
 |
 |
|
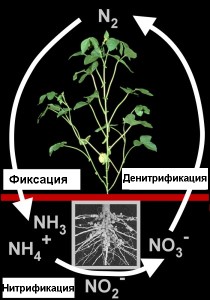
2. Биологический круговорот азота в почве состоит из a) фиксации азота бактериями, которые могут жить в симбиозе с растениями (как на корнях сои) и b) денитрификации другими бактериями, которые выделяют молекулярный азот или N2O при распирации. Щелкните для увеличения. (50 KB)
Коллаж: Elmar Uherek
|
|
|
Денитрификация является процессом разложения нитрата с получением азота. Это выполняется микроорганизмами (палочковидная бактерия, псевдомонас и другие бактерии), которые при усвоении переключаются от кислорода к нитрату, в особенности в недостаточно проветриваемых почвах. Процесс денитрификации может привести к нескольким промежуточным продуктам. Наиболее важный – закись азота. Газы возвращаются в атмосферу. Закись азота – долгоживущий парниковый газ.
Фиксация азота является процессом, противоположным денитрификации.
|
 |
 |
|
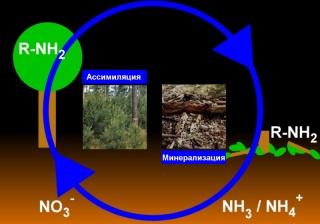
3. Ассимиляция и минерализация определяет поглощение соединений азота из почвы и объединение их в биомолекулы растений, и конверсию в неорганическй азот после отмирания растений, соответственно. Щелкните для увеличения. (70 KB)
Схема: Elmar Uherek
|
|
 |
 Ассимиляция и минерализация Ассимиляция и минерализация
Усваемые соединения азота могут накопляться в почве в неорганической форме (нитрат) или могут быть включены в живой организм как органический азот.
Ассимиляция – переход неорганического азота (типа нитрата) в органическую форму азота как, например, аминокислоты. Нитрат переходит с помощью ферментов сначала в нитрит (редуктаза нитрата), затем в аммиак (редуктаза нитрита). Аммиак входит в состав аминокислот.
|
Минерализация (аммонификация) это процесс, в течение которого редуценты, такие как земляные черви, термиты, слизняки, улитки, бактерии и грибы преобразовывают органический азот отмерших растений в неорганические формы. Первый шаг это формирование аммиака и его солей (NH4+X-).
Ассимиляция и минерализация являются противоположными процессами.
|
 |
 |
 |
|
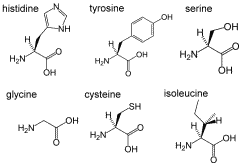
4. Аминокислоты – это азот, содержащийся в биомолекулах. Из аминокислот образуются протеины.
|
|
|
 Атмосферное окисление Атмосферное окисление
Самые важные пути естественного производства оксидов азота это окислительные процессы при высоких температурах. Это может быть при высокой температуре лесных пожаров или при окислении молекулярного азота (инертного в нормальных условиях) при извержениях вулкана или при разрядах молнии.
Главными продуктами таких процессов являются оксид азота, NO, и диоксид азота, NO2, а после дальнейших реакций – азотная кислота. Как было сказано в тексте “Исследования”, определенные концентрации NO и NO2 приводят к формированию озона при помощи солнечного света и эмиссии углеводородов.
|
 |
 |
|
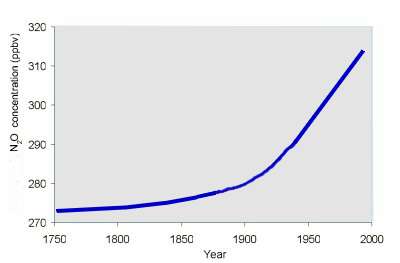
5. Увеличивающаяся фракция закиси азота (веселящий газ) в воздухе– прежде всего, последствие употребления азотных удобрений. Диаграмма: Elmar Uherek
|
|
 |
 Влияние человеческой деятельности Влияние человеческой деятельности
Оксиды азота и озоновый смог
В дополнение к естественным источникам, люди ответственны за эмиссию NO / NO2 в результате горения при технических процессах. Самое распространенное – это горение в автомобильных двигателях. При определенных условиях если средние концентрации в воздухе становятся слишком высокими, это может привести к озоновому смогу.
Кроме того, оксиды азота в атмосферных реакциях преобразовываются в азотную кислоту, что вносит свой вклад в кислотные дожди и к их отрицательным последствиям.
|
Внесение удобрений и эвтрофикация
Чтобы улучшать условия для растущих зерновых культур, в почву вносятся азотосодержащие удобрения. Это можно бы назвать технической фиксацией азота, базируемой, например, на синтезе аммиака в процессе Габера-Боша.
|
 |
|
 |
 |
|
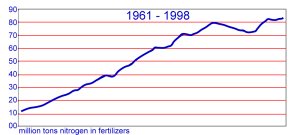
7. Рост производства азотосодержащих удобрений очень увеличился за последние десятилетия. График от IFA.
|
|
 |
Если внесено слишком много удобрений и излишек не принят растениями, это вызывает двойное отрицательное действие. Аммиак и нитраты смываются в водоемы и прибрежные зоны. Здесь они вызывают сильный рост растений и морских водорослей (фитопланктона), и в результате жизнь в воде может быть погашена, так как содержание кислорода будет уменьшаться из-за разложения отмирающих растений.
|
|
Кроме того, денитрификация увеличивается и производится больше закиси азота N2O. Это увеличивает парниковый эффект, а закись азота, достигающая стратосферы, преобразовывается в другие оксиды азота, способствующие истощению озонового слоя.
|
Автор:
Elmar Uherek - Max Planck Institute for Chemistry, Mainz
|
|
 |
|







