|
|
 |
|
|
|
 |
| |
|
|
 |
A alta atmosfera
Básico |
A composição da Estratosfera
A maioria dos compostos libertados à superfície da Terra não atinge a estratosfera. Eles podem ser:
decompostos por gases atmosféricos na troposfera (pelos principais oxidantes, e.g. OH, NO3, ozono)
destruídos pela luz solar
removidos por deposição seca ou húmida
retidos na fria tropopausa.
|
|
|
|
|
 |
Devido à inversão na evolução da temperatura com a altitude entre a troposfera e a estratosfera, as transferências de ar entre estas duas camadas são lentas. Na troposfera as transferências verticais demoram entre várias horas a vários dias, enquanto que na estratosfera a mistura ocorre em escalas temporais da ordem de meses a anos.
|
A primeira consequência é que o teor em vapor de água na estratosfera é muito baixo. As razões de mistura (ver definição em baixo) típicas são da ordem de 2 a 6 ppm (partes por milhão), enquanto na baixa troposfera são da ordem de 1.000 a 40.000 ppm e de 100 ppm na alta troposfera. Assim, a formação de nuvens estratosféricas é rara e as temperaturas terão de ser muito baixas para que os cristais de gelo se formem. Tais condições existem nas regiões polares, onde podem existir as nuvens estratosféricas de gelo. Devido ao tráfego aéreo, por exemplo, o teor em vapor de água na estratosfera aumenta; por outro lado, a temperatura tem aumentado devido ao aquecimento da troposfera. Assim, não é de excluir a hipótese de que a formação das nuvens estratosféricas polares (em inglês PSC) seja cada vez mais frequente.
|
 |
 |
 |
|
1. Nuvens estratosféricas polares sobre Kiruna / Sweden
fonte: MPI Heidelberg - (35 K)
|
|
Os compostos inorgânicos na estratosfera
A química estratosférica é dominada pelo ozono (cuja fórmula é O3). 85% a 90% do ozono atmosférico encontra-se na estratosfera. Este gás forma-se na estratosfera, a partir do oxigénio (O2 ), por acção do sol (fotólise). Fotólise significa que a radiação solar quebra as ligações entre os átomos de oxigénio da molécula O2 . A maioria dos gases que entra na estratosfera são:
gases com uma longa duração de vida que provém da troposfera (por exemplo o óxido de azoto, N2O, o metano, CH4, os clorofluorcarbonetos CFC, etc...)
ou gases que são injectados por erupções vulcânicas fortes (compostos de enxofre, aerossóis).
Assim, os compostos inorgânicos são os dominantes na composição da estratosfera: óxidos de nitrogénio, ácido nítrico, ácido sulfúrico, ozono, halogénios e os óxidos de halogénio resultantes da destruição dos CFC.
|
 |
 |
|
2. Erupção do Monte Pinatubo, nas Filipinas, em Junho de 2001.
fonte: Cascades Volcano Observatory USGS Fotografia de Rick Hoblitt
|
|
 |
As erupções vulcânicas
Grandes erupções vulcânicas podem injectar directamente na estratosfera enormes quantidades de gases e de partículas. Estes gases podem ser ácidos de halogénio como HCl e HF ou dióxido de enxofre, SO2, que oxidando origina o ácido sulfúrico H2SO4 (um composto fundamental na formação das nuvens). As partículas (principalmente material inorgânico como silicatos, sais haletos e sulfatos) podem absorver a luz solar na estratosfera, e provocar um aquecimento temporário da estratosfera e um arrefecimento da troposfera. Estes efeitos podem fazer-se sentir durante 1 a 2 anos após as erupções, e podem ser medidos sobre todo o hemisfério, como sucedeu após a erupção do Monte Pinatubo, em Junho de 1991.
|
Compreender as concentrações e as razões de mistura
A quantidade de um composto na atmosfera pode exprimir-se de duas formas - através de uma quantidade relativa ou de uma quantidade absoluta:
a) razão de mistura = fracção do composto entre todas as moléculas de ar. Se existirem 40 moléculas de ozono em 1 milhão de moléculas de ar, a razão de mistura será 40 partes por milhão (40 ppm). Esta é uma quantidade relativa.
b) concentração = massa de moléculas do composto existente num determinado volume de ar. Se existirem 100 µg (micrograma) de ozono em 1 metro cúbico de ar, a concentração é de 100 µg / m3. Esta é uma quantidade absoluta.
Conhecendo a pressão, podemos converter um dos valores no outro.
A pressão decresce com a altitude, i.e. quanto mais alto subimos na estratosfera, menos moléculas existem por metro cúbico de ar. Ou seja, se a massa absoluta de ozono se mantiver constante com a altitude, a quantidade relativa de ozono entre as outras moléculas de ar (razão de mistura) aumenta.
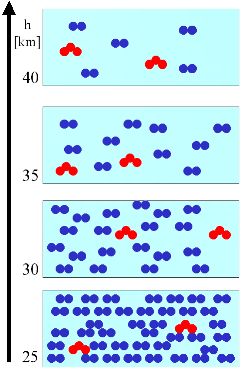
Este princípio geral explica-se, em baixo, através de um exemplo muito simples. Num determinado volume de ar (caixa em azul claro) existe um certo número de moléculas de ar (representadas em azul, para simplificar, apesar de o ar ser uma mistura de diversos gases) e um certo número de moléculas de ozono (representadas em vermelho). O número de moléculas que constituem o ar decresce com a altitude em qualquer dos casos.
|
 |
 |
|
3. (L1) Aqui admitimos que a quantidade de moléculas de ozono (círculos a vermelho) [concentração = moléculas/volume = massa/volume, unidade e.g. molec./m3, hPa, µg/m3] permanece constante com a altitude (triângulos a vermelho no perfil). Uma vez que o número de moléculas que constituem o ar (círculos a azul) diminui, a razão de mistura [unidade e.g. %, ppm, ppb, ppt] do ozono aumenta (ver figura em baixo).
|
|
 |
 |
 |
|
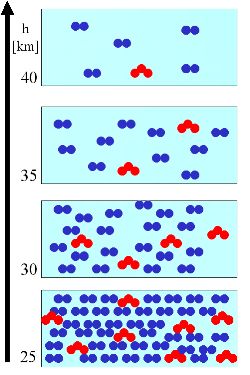
3. (R1) Neste caso admitimos que a quantidade de moléculas de ozono decresce com a altitude, da mesma forma que a quantidade de moléculas que constituem o ar. Assim, a razão de mistura (número de moléculas de ozono por moléculas de ar) mantém-se constante com a altitude (símbolos a verde): 8/40, 4/20, 2/10, 1/5 = 20%. Mas o valor absoluto de moléculas de ozono por volume de ar diminui (triângulos a vermelho).
|
|
|
O que se passa na realidade ?
Entre a superfície e a baixa estratosfera é o exemplo da esquerda que melhor descreve a realidade. Neste caso a concentração de ozono mantém-se aproximadamente constante, mas como o ar circundante se torna rarefeito com a altitude, a razão de mistura aumenta.
Na baixa estratosfera existe mesmo um aumento da concentração de ozono (a figura em baixo mostra um aumento por um factor de oito). Assim, o exemplo da direita é realista na região superior da camada do ozono.
|
|
|
 |
Em publicações tanto poderá encontrar o perfil indicado a vermelho, como o indicado a verde, como até ambos os perfis. Mas convém lembrar que as proporções não são de 1 molécula de ozono para 5 moléculas de ar, mas de 1 molécula de ozono para 1 milhão de moléculas de ar [1ppm].
4. Fig. à esquerda: evolução do ozono com a altitude (perfis de concentração e de razão de mistura)
fonte: adaptado de IUP Bremen
|
Acerca desta página:
Autor: Dr. Elmar Uherek, MPI for Chemistry, Mainz
Revisão científica: Dr. John Crowley, MPI for Chemistry, Mainz - 2004-05-04
Revisão educacional: Michael Seesing - Univ. of Duisburg, Dr. Ellen K. Henriksen - Univ. of Oslo, Yvonne Schleicher - Univ. of Erlangen-Nürnberg
Versão portuguesa: Margarida L. R. Liberato - Dep. de Física, UTAD, Portugal
Última actualização: 2004-05-05
|
|
 |
|







