|
|
 |
|
|
|
 |
| |
|
|
 |
Obere Atmosphäre
Basis |
Bildung von Ozon
Die Biosphäre, das Dasein der Tiere auf unserem Planeten und natürlich auch menschliches Leben wurde erst ermöglicht durch die Bildung von Ozon in der Stratosphäre. Ozon schützt uns vor der UV-C und UV-B Strahlung der Sonne (Licht mit Wellenlängen von kleiner 320 nm), das Biomoleküle schädigt. In der Erdgeschichte konnte sich Ozon nach der Freisetzung von Sauerstoff in die Atmosphäre etwa zwischen 2000 und 600 Millionen Jahren vor der heutigen Zeit bilden. Aber wie?
|
|
|
|
|
 |
 |
 |
|
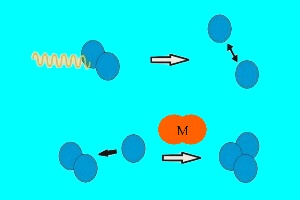
1. Die Photosynthese von Ozon - Lichtspaltung von Sauerstoff führt zur Bildung des O3 Moleküls
|
|
 |
UV Licht führt zur Ozonbildung und zu seinem Abbau
In der Stratosphäre gibt es zwei stabile Formen des Sauerstoffes: normalen Luftsauerstoff O2, der aus zwei O Atomen besteht und Ozon O3, welches aus drei O Atomen besteht. Um die eine Form in die andere zu überführen, ist intensives UV-Licht notwendig. Die O-O Bindung in einem Sauerstoffmolekül wird gebrochen. Das gebildete O Atom reagiert mit weiterem Sauerstoff (aus Gründen der Energieabgabe unter Stoß mit irgendeinem dritten Partner M) und es bildet sich Ozon.
|
 |
 |
|
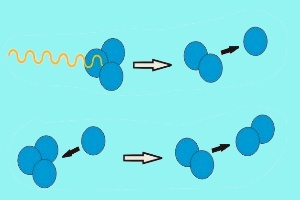
2. Photolyse von Ozon - Abbau durch Lichtspaltung
|
|
 |
Das hierzu nötige UV-Licht (gelbe Welle) kommt von der Sonne.
In vergleichbarer Weise wird das Ozon auch durch Photolyse (= Lichtspaltung) wieder abgebaut, wenn die O-O Bindung in einem Ozonmolekül durch das Sonnenlicht gebrochen wird. Das gebildete O Atom reagiert mit einem anderen Ozon Molekül und bildet zwei Moleküle normalen Sauerstoffs O2.
|
Bildung in den Tropen, Anreicherung an den Polen
Da die Sonneneinstrahlung über den Tropen am stärksten ist, wird hier die größte Menge des weltweiten Ozons gebildet. Die tropische Sonne treibt aber nicht nur die Ozonbildung an, sondern auch den Aufstieg troposphärischer Luft in große Höhen.
Ozon wird von Äquator weg transportiert in Richtung der Pole, wo es sich in der kalten subpolaren Region sammelt. Am Äquator selbst sind sowohl Ozonbildung als auch sein Abbau sehr hoch. Dort kann sich Ozon nicht sammeln. In den subpolaren Regionen jedoch ist der photochemische Abbau gering und der Transport vom Äquator eine wichtige Quelle. Die Werte an den Polen selbst sind etwas niedriger, insbesondere im Winter, wenn während der Polarnacht kein weiteres Ozon gebildet werden kann. Insgesamt also findet man die höchsten Ozonkonzentrationen über der weiteren polaren Region, solange dieses System nicht durch die Bildung eines Ozonloches gestört wird wie im antarktischen Frühling.
|
 |
 |
 |
|
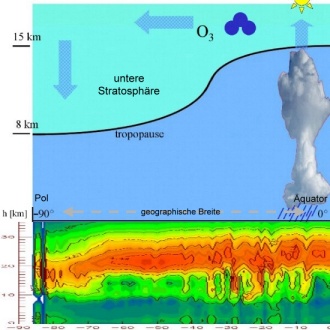
3. Die Abbildung zeigt den Ozontransport gemäß der beschriebenen Theorie. Der Querschnitt durch die Atmosphäre unten zeigt die gemessene Ozonverteilung zwischen den Polen und dem Äquator (niedrige Werte = blau, hohe Werte = rot). Man sieht, dass in der Nähe des Äquators ozonarme Luft aus der Troposphäre in große Höhen vorstößt.
Daten von GOME (DLR, IUP Bremen) - Bitte Bild zum Vergrößern anklicken! (100K)
|
|
 |
 |
|
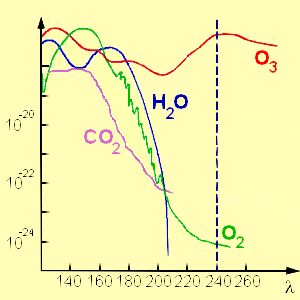
4. Die Absorption von Ozon im Vergleich mit anderen atmosphärischen Verbindungen, die im UV Bereich des Sonnenlichtes absorbieren.
Überarbeitung einer Originalgrafik von:  Chemie Didaktik Uni Wuppertal (vormals Uni Duisburg) Chemie Didaktik Uni Wuppertal (vormals Uni Duisburg)
|
|
 |
Ozon absorbiert UV-Licht
In derselben Weise wie UV Licht für die Ozonbildung notwendig ist, wird es auch wieder durch die Ozonmoleküle aufgenommen (= absorbiert). Dies hat drei Konsequenzen:
1) Das Licht erreicht die unteren Teile der Atmosphäre nicht, sodass die Erdoberfläche geschützt ist.
2) Die Menge an Ozon, die sich anreichern kann, ist begrenzt. Denn mit steigender Ozonkonzentration steigt auch die Wahrscheinlichkeit eines Abbaus. Dies führt zu einem Gleichgewicht.
3) UV Licht enthält viel Energie. Diese Energie wird in Wärmestrahlung überführt und heizt so die Stratosphäre auf. Darum kommt es zur Umkehr des Temperaturtrends an der Tropopause.
|
Die Dicke der Ozonschicht
Der Begriff Ozon'schicht' wird häufig missverstanden. Der Begriff bedeutet, dass es in der Stratosphäre einen Bereich der Luft zwischen 18 und 40 km Höhe gibt, in dem die Konzentration und das Mischungsverhältnis an Ozon deutlich höher sind, als in der Troposphäre darunter und in der Mesosphäre darüber. Der Anteil Ozon ist jedoch immer noch sehr, sehr gering im Vergleich mit Stickstoff und Sauerstoff. Nicht mehr als 10 Moleküle unter einer Million sind Ozon. Weil es aber in der Troposphäre noch weniger ist, befinden sich 90% aller Ozonmoleküle in der Stratosphäre und wir sprechen darum von einer Ozonschicht. Die Ozonschicht darf man sich aber nie als eine Schicht im Sinne eines dünnen Films aus reinem Ozon vorstellen.
|
Dobson units (DU)
Die Ozonmenge wird, anstelle einer Konzentration oder eines Mischungsverhältnisses, gerne auch in Dobson Einheiten (Dobson Units = DU) angegeben. 300 DU ist ein typischer Wert. Aber was heißt das? Nehmen wir an, die Ozonmoleküle wären nicht über die ganze Stratosphäre und 10% ja auch über die Troposphäre verteilt, sondern in einem dünnen Film am Erdboden konzentriert. Und bestände dieser Film aus reinem Ozon, so wäre er etwa 3 mm dick (= 300 DU). Also: 1 DU = 0,01 mm Dicke eines gedachten Filmes aus reinem Ozon am Erdboden.
|
 |
|
 |
 |
|
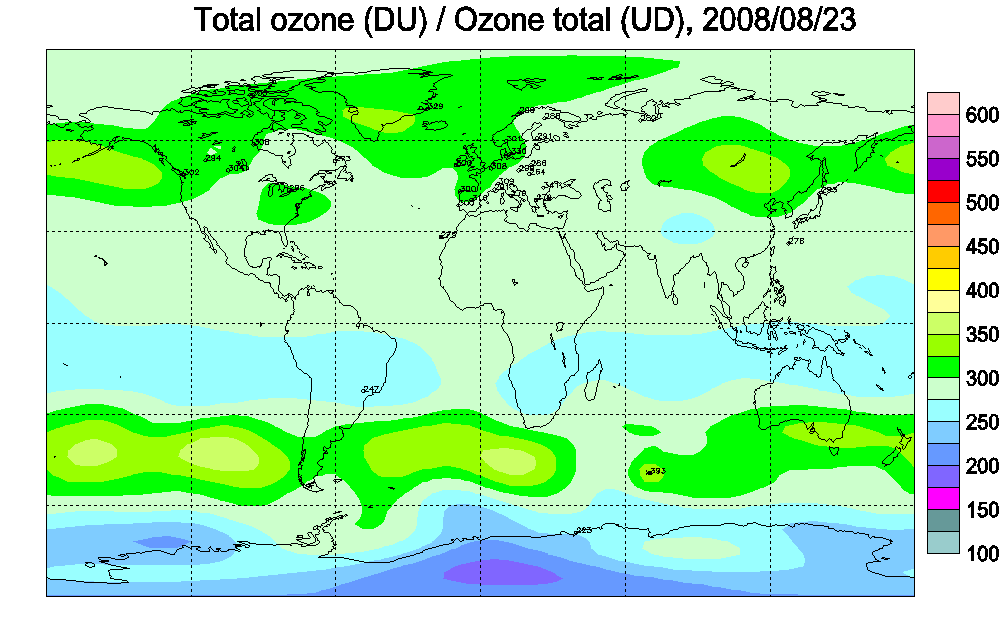
6. Aktuelle Ozonkarte, bereitgestellt vom kanadischen Wetterdienst.
Zum Vergrößern bitte das Bild anklicken!
|
About this page:
author: Dr. Elmar Uherek - Max Planck Institute for Chemistry, Mainz
educational proofreading: Michael Seesing - Univ. of Duisburg - 2003-07-02, Dr. Ellen K. Henriksen - Univ. of Oslo
scientific reviewer: Dr. John Crowley - MPI Chemistry, Mainz 2004-05-06
educational reviewing: Hendrik Förster & students, Nordpfalz Gymnasium Kirchheim-Bolanden - March 2004
Letzte Überarbeitung: 2007-08-23
|
|
 |
|







