|
|
 |
|
|
|
 |
| |
|
|
 |
Untere Atmosphäre
Mehr .. |
3. Ozon und Feuer - Mehr
Arbeitsblatt 1:
Ozon und seine chemischen Eigenschaften
|
|
|
|
|
 |
|
A 1 |
Formuliere zu der unten angegebenen Grenzstruktur des Ozon-Moleküls eine zweite Grenzstruktur! |
|
|
|
A 2 |
Wie ist der Dipol-Charakter des O3-Moleküls zu erklären? Vergleiche mit den Molekülen CO2 und H2O! |
|
A 3 |
Bei der Reaktion von Ozon mit einem Alken (Ozonolyse) wird das Alken-Molekül an der C=C Doppelbindung gespalten. Es bilden sich in mehreren Reaktionsschritten zwei Carbonylverbindungen. Formuliere und benenne die Produkte bei der Ozonolyse von
a) 2-Buten und
b) 2-Methyl-2-buten!
|
Einige Eigenschaften von Ozon:
|
|
|
l Siedepunkt = -112.5° C |
l schlecht wasserlöslich |
|
l Schmelzpunkt = -251.4° C |
l löslich z.B. in CF2Cl2 |
|
l Dipolmoment µ = 0.49 D |
l giftig |
|
l bläuliche Farbe |
l O2/O3 (w (O3) < 10% bis T < 100° C beständig |
|
l charakteristischer Geruch |
l O3(s), O3(l) explodiert bei Berührung |
Starkes Oxidationsmittel:
|
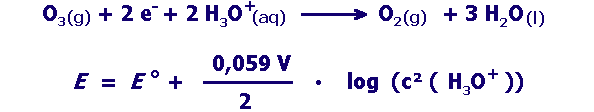 |
 |
|
E° = 2,07 V
Beispiele für Oxidationsreaktionen mit Ozon
|
|
|
A 4 |
Verläuft die Oxidation durch Ozon besser bei hohem oder niedrigem pH-Wert? Begründe mit Hilfe der geeigneten Angaben aus dem Kasten oben. |
|
A 5 |
Iodid-Ionen können auch durch molekulares Chlor oxidiert werden. Formuliere die Reaktion und erläutere, welcher Unterschied dennoch zur Reaktion 1 aus dem Kasten besteht. |
|
|
In der Atmosphäre wird in Wolkentröpfchen Schwefelige Säure (Schwefeldioxid in Wasser) durch Ozon oxidiert. Diese Oxidation wird von hohen pH-Werten begünstigt.
|
About this page:
Authors: M. Seesing, M. Tausch - Universität Duisburg-Essen, Duisburg / Germany
Scientific reviewer: Dr. Rolf Sander - Max Planck Institute for Chemistry, Mainz - 2004-05-18
Last update: 2004-05-24
|
|
 |
|







