|
|
 |
|
|
|
 |
 |
|
|
 |
Contexte: Condensation
|
Mots clés:
évaporation, condensation, saturation, nucléation, formation de particules | |
 |
 |
|
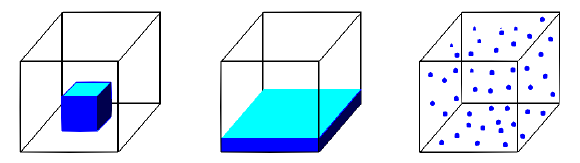
1. SOLIDE - LIQUIDE - GAZEUX
Les trois états de la matière.
Graphique emprunté à la NASA.
|
Nous savons que l’eau, tout comme d’autres substances chimiques, peut changer d’état, selon la température. Au point de fusion, la glace fond. Au point d’ébullition, l’eau s’évapore. Nous savons aussi que l’eau s’évapore déjà en-dessous du point d’ébullition.
Dans l’atmosphère, les substances ne changent pas seulement d’état physique. Elles réagissent aussi chimiquement. De nouvelles molécules sont produites. Il peut ainsi arriver que la température ambiante soit inférieure à la température de fusion de ces nouvelles substances, pourtant produites sous forme gazeuse ! Que se passe-t-il alors avec ces gaz ?
|
 |
 |
 |
|
2. La condensation d’air humide dans les couches hautes et froides de l’atmosphère conduit à la formation de nuages et parfois de pluie.
Clique sur l'image pour l'agrandir! (325 Ko)
© Earth Science Australia
|
|
De telles molécules ne tombent pas tout de suite au sol. Elles flottent dans l’air. Elles peuvent rencontrer d’autres grosses molécules et former des paires ou des groupes de molécules. Le processus continue jusqu’à former des agrégats. C’est le premier pas de la "nucléation" (= formation de noyaux) et de la formation de particules. On pourrait presque dire qu’il s’agit simplement de condensation et de (re-)sublimation. Mais la réalité est plus complexe, car il ne s’agit pas d’une substance pure, mais d’un mélange de différentes espèces chimiques.
Des agrégats de molécules qui flottent dans l’air sont nommés particules ou aérosols. Si ces agrégats sont composés d’eau solide ou liquide, on parle de cristaux de glace et de gouttelettes ou de gouttes. Plus les particules sont petites, plus elles flottent longtemps dans l’air, avant de se déposer sur le sol. D’innombrables particules liquides et solides flottent en permanence dans l’air qui nous entoure.
|
 |
 |
 |
|
Particules de suie collectées sur un filtre (les grands points noirs sont les pores du filtre).
Les particules ne sont pas toutes formées chimiquement dans l’air. Certains aérosols sont directement injectés dans l’atmosphère : poussières des tempêtes de sable, suie des gaz d’échappement automobiles, sel de mer émis par l’écume, etc.
Clique sur l'image pour l'agrandir! (80 Ko)
© Max-Planck-Institut für Chemie Mainz - AG Helas
|
|
 |
 |
|
4. a) Deux molécules d’eau (H2O) se rencontrent dans l’atmosphère. Elles ont trop d’énergie (symbolisée par une flèche jaune), qui ne peut pas être transmise à un autre corps. Elles se séparent donc automatiquement.
|
|
 |
L’air peut contenir de la vapeur d’eau, mais pas au-delà d’un maximum, qui dépend de la température. Lorsque l’eau s’évapore (d’un lac, d’une mer, du sol, etc.), l’humidité de l’air augmente. Quand le contenu en vapeur d’eau dans l’air est maximal, l’humidité est de 100%.
Plus l’air est froid, moins il peut contenir d’eau. Conséquence : lorsque de l’air humide et chaud s’élève dans l’atmosphère, il refroidit. Sa pression de saturation diminue, en dessous de son contenu en vapeur d’eau (son humidité relative dépasse 100%). La vapeur condense et les gouttelettes forment des nuages (figure 2).
Mais la vapeur d’eau ne suffit pas à la formation de nuages...
|
 |
 |
|
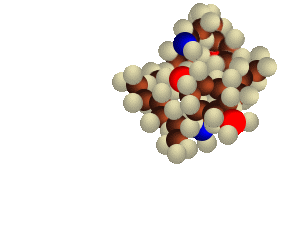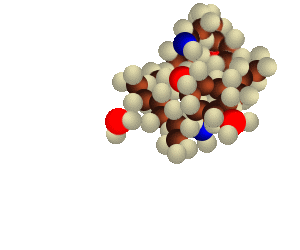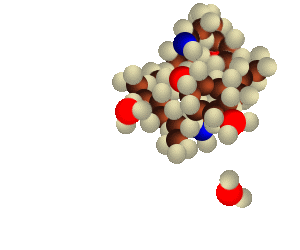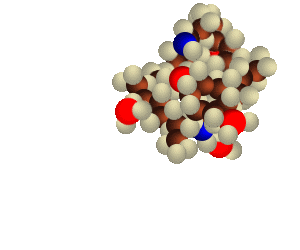
4. b) Lorsque des molécules d’eau rencontrent une particule, cette dernière peut facilement absorber leur énergie sous forme de déformation ou d’oscillation (de la particule). Les molécules d’eau adhèrent donc à la surface de la particule qui grandit ainsi.
Animation: © Elmar Uherek
|
|
 |
À l’état gazeux, les molécules d’eau possèdent une grande énergie (qui leur a été transférée lors du processus d’évaporation). Lorsque deux molécules se rencontrent dans l’atmosphère, même si cette dernière est saturée, elles ont trop d’énergie pour rester ensemble. Les molécules ne peuvent pas se débarrasser de cette énergie et se séparent tout de suite après la rencontre. On pourrait comparer les molécules d’eau (vapeur) à des balles de caoutchouc légèrement collantes. Si deux balles sont lancées l’une contre l’autre à grande vitesse, elles rebondissent et se séparent. Par contre, si elles sont lancées contre un grand ballon mou, elles s’y enfoncent et y reste collées.
Dans de l’air absolument exempt de particules, aucune goutte d’eau ne pourrait se former, même si l’humidité relative est de 200%. Mais l’atmosphère réelle contient toujours des particules. Les molécules d’eau les heurtent, y perde leur énergie et y adhèrent. D’autres molécules y adhèrent ensuite, et ainsi de suite, jusqu’à former une gouttelette. Les nombreuses gouttelettes et gouttes forment alors brouillard et nuages.
|
|
 |
|







