|
|
 |
|
|
|
 |
| |
|
|
 |
Klima i byer
Les mer |
Opphavet til sur nedbør
Sure forbindelser faller ned til bakken både som nedbør (regn, snø, hagl) og som tørre partikler. Svoveldioksid (SO2) og nitrogenoksider (NOx-gasser) reagerer med vanndamp i lufta og danner svovelsyre og salpetersyre. Andre stoffer, som flyktige organiske forbindelser (VOC), bidrar også til sur nedbør.
|
|
|
|
|
 |
|
En nærmere titt på pH
I kapittelet Hva er sur nedbør? i innføring-delen [link] beskriver vi pH som et mål på surhetsgraden i en løsning er. pH-skalaen ble utviklet av Søren Sørenson (laboratorieleder ved Carlsberg bryggerier) i 1909 og pH-verdien til en løsning er gitt ved:
pH = -log[H+]
der [H+] er konsentrasjonen av hydrogenioner (protoner).
pH-skalaen er bygget på at enkelte vannmolekyler selv i rent vann spaltes i ioner; hydrogenionet (H+) og hydroksidionet (OH-). Denne prosessen kalles egen-protolyse. Deretter forbinder hydrogenionene seg med vannmolekyler og danner oksoniumoner (H3O+).

Reaksjonen er reversibel. Produktene på høyre side av pila kan reagere tilbake til de opprinnelige vannmolekylene på venstre side. Forholdet mellom produktene (H3O+ og OH-) og de to H2O-molekylene er alltid konstant. Denne konstanten kalles ioneproduktkonstanten for vann, Kw, og har verdien 10-14.
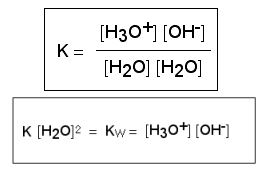
Kw = [H3O+] [OH-] = 10-14
Hvis vi setter inn logaritmene i denne likningen, får vi: pKw = pH + pOH = 14
Den lille p-en står her for en potens med grunntall 10 (10x). Hvis f eks [H3O+] er 1,0 x 10-5 mol/L, er pH = 5.
I rent vann [H3O+] = [OH-] = 10-7 mol/L og pKw = 7 + 7 = 14
Fordi Kw har en konstant verdi, kan vi bestemme om en løsning er sur eller basisk ved å se på de relative andelene H3O+ og OH- i løsningen:
Sur løsning: [H3O+] > [OH-]
Nøytral løsning: [H3O+] = [OH-]
Basisk løsning: [H3O+] < [OH-]
|
|
Oppdagelsen av problemet med sur nedbør
Sur nedbør ble første gang betraktet som et problem så langt tilbake som på slutten av 1600-tallet. I 1692 ga Robert Boyle ut boka A general history of the air, der han omtalte fenomenet uten å kalle det sur nedbør. Begrepet ble først tatt i bruk i 1872 av forskeren Robert Angus Smith (1817-1884) i boka Air and Rain: The beginnings of Chemical Climatology. Men det var ikke før på 1960-tallet at det store problemet med sur nedbør ble oppdaget. Undersøkelser viste at surhetsgraden i innsjøer i Skandinavia og Nord-Amerika var økende og at fiskepopulasjonene ble mindre og skogene døde. Som et resultat av disse vitenskapelige undersøkelsene, ble det tatt politiske avgjørelser for å forsøke å minske problemet med sur nedbør.
|
|
Menneskeskapte utslipp som en kilde til sur nedbør
I tillegg til utslipp av svoveldioksid og nitrogenoksider fra forbrenningen av fossilt brennstoff, er det også andre stoffer som bidrar til dannelse av sur nedbør. Blant disse stoffene er hydrogenklorid og organiske syrer. To av disse organiske syrene er eddiksyre og maursyre. De organiske syrene oppstår i lufta når flyktige organiske forbindelser oksiderer. Disse forbindelsene har både menneskeskapte og naturlige kilder. De menneskeskapte utslippene stammer først og fremst fra eksos fra kjøretøy, mens den viktigste naturlige kilden er planter. De naturlige kildene står for omlag ti ganger så mye av utslippene av flyktige organiske forbindelser som de menneskeskapte kildene.
|
|
Dobbeltrollen til ammoniakk
Ammoniakk (NH3) er også en svært viktig gass i atmosfæren. Det er en basisk gass som reagerer med syrer i lufta og danner ammonium-ioner (NH4+). Ammoniakkgass reagerer med svovelsyre og danner saltpartikler av ammoniumsulfat
(NH4)2SO4. Ammoniakk kan også reagere med salpetersyre og danne saltpartikler av NH4NO3. Disse reaksjonene nøytraliserer syrene og reduserer derfor luftas surhetsgrad. Men når saltpartiklene når bakken, reagerer de med oksygen og kan sette i gang en prosess som kalles nitrifikasjon:
NH4+ + 2 O2 -> 2 H+ + NO3- + H2O
I denne prosessen frigjøres hydrogenioner. Nedfall av ammonium og den etterfølgende nitrifikasjonen får derfor som direkte konsekvens at jordsmonnet forsures. |
 |
 |
|
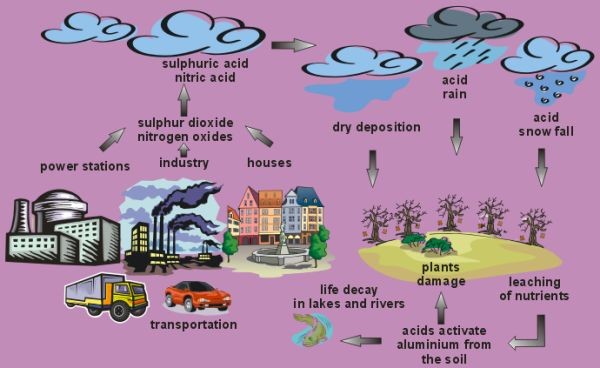
1. Kilder til og virkninger av sur nedbør og andre typer surt nedfall.
Forfatter: Sebastian Wypych.
|
|
Nedfall
Nedfall er det som skjer når kjemiske forbindelser i atmosfæren faller til jordoverflaten.
|
|
Vått nedfall
Prosessen der kjemiske forbindelser forflyttes fra lufta til jordoverflaten via vann (regn, sludd, snø, hagl eller tåke) kalles vått nedfall. De forbindelsene som står for mesteparten av den sure nedbøren, er svovelsyre og salpetersyre. Disse syrene dannes i lufta fra gassene svoveldioksid (SO2) og nitrogenoksider
(NO og NO2). Forbrenning av kull og olje i energiverk for å produsere elektrisk strøm er en viktig kilde for begge disse gassene. Eksos fra biler er en annen viktig kilde til utslipp av nitrogenoksider. Gassene reagerer med hydroksylradikalet (OH) og oksygenatomer (O) og danner syrene. Sure partikler er svært hygroskopiske (de absorberer vann lett) og kan lett opptre som kondensasjonskjerner, og dermed øke skydannelse. Når disse skyene avgir nedbør, er det surt regn som når bakken. På veien mot bakken kan regndråpene ta med seg flere sure partikler og på den måten øke surhetsgraden sin ytterligere..
|
 |
 |
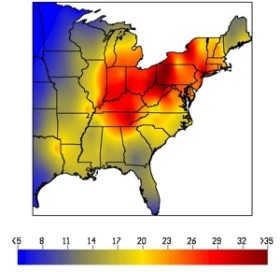
2. Trender i vått nedfall av sulfat (kg ha-1) i østlige USA fra NADP/NTN Monitoring Data. Bildet til venstre viser data for perioden 1989- 1991, mens bildet til høyre viser data for perioden 1995- 1998. På det tidlige 90-tallet, var vått nedfall av sulfat høyest i et stort område av det midtvestlige og østlige USA, inkludert Ohio River Valley, Western Pennsylvania og de sentrale Appalachiske fjell (se 1989-1991).
|
|
 |
 |
 |
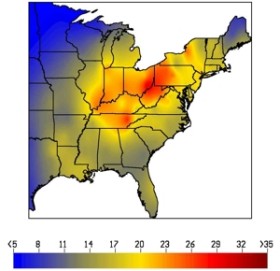
Som et resultat av betydelige reduksjoner i svoveldioksidutslipp fra 1995 (Fase 1 i Sur Nedbør Programmet), sank svovelnedfallet i regn med opp til 25% over et stort område av det østlige USA. Denne reduksjonen var enestående i omfang og geografisk utstrekning (se 1995-1998). Kilde: U.S. Environmental Protection Agency
http://www.epa.gov/airmarkets/cmap/
mapgallery/mg_wetsulfate.html |
|
|
Tørt nedfall
Surt nedfall treffer jordoverflaten hele tiden, ikke bare når det er nedbør. Når syregasser og sure partikler i atmosfæren faller ned på bakken, kalles det tørt syrenedfall Hvis gassene og partiklene kommer ned i vann og vassdrag, kan de forårsake forsurning. Hvis de treffer planter og bygninger kan de skade dem direkte. Omlag halvparten av atmosfærens syreinnhold kommer ned på jorda som tørt nedfall.
|
|
Gasser og partikler som avsettes tørt på trær og andre overflater, kan vaskes vekk av regn. Når dette skjer, øker vannets surhetsgrad ytterligere. Tørt nedfall forekommer vanligvis i nærheten av utslippskilden, mens vått nedfall kan falle ned inntil tusen kilometer unna utslippskilden. Bruk av høye fabrikkpiper for å spre forurensningen har forbedret luftkvaliteten i industrialiserte områder drastisk. Men forbedringen av luftkvaliteten lokalt ved utslippskildene har også hatt sin pris luftforurensning blåser nå med vinden over store avstander og påvirker mye større områder. På grunn av denne lange transporten fører sur nedbør ofte til større problemer enn tørt syrenedfall.
|
Om denne siden:
Forfattere: Anita Bokwa - Jagiellonian University, Cracow, Poland and Dr. Elmar Uherek - Max Planck Institute for Chemistry, Mainz, Germany
Vitenskapelig kvalitetssikring: Kimitaka Kawamura - Hokkaido University, Sapporo, Japan - 2004-08-12
Pedagogisk kvalitetssikring: Michael Seesing - University of Duisburg, Duisburg, Germany
Sist oppdatert: 2004-08-17
Oversatt og bearbeidet av Nicolai Steineger og Erik Steineger
|
|
 |
|







