|
|
 |
|
|
|
 |
| |
|
|
 |
Klima i byer
Innføring |
Hva er sur nedbør?
Vann er essensielt for livet på jorda. Når vannet blir forurenset, får det derfor betydning for hele miljøet. Sur nedbør skyldes for det meste menneskeskapte utslipp av luftforurensning ved forbrenning av fossilt brennstoff. Syreholdigheten i regnet kan måles ved hjelp av pH-skalaen. |
|
|
|
|
 |
|
Atmosfærisk nedbør (regn, yr, snø, osv.) siver inn i jordsmonn og elver eller fordamper og blir til vanndamp. Et viktig verktøy for å beskrive vannkvalitet er pH-verdien.
|
 |
 |
|
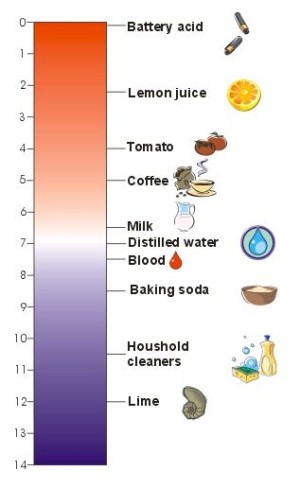
1. pH-skalaen. Typisk pH-verdi på noen husholdningsvarer. Jo lavere verdien er, jo høyere er surheten.
Forfatter: Sebastian Wypych
|
|
 |
pH-skalaen
I naturen finner vi mange kjemiske forbindelser oppløst i vann, som danner vannoppløsninger med en bestemt pH-verdi. Jo surere vannoppløsningen er, jo lavere er pH-verdien.
pH er den negative logaritmen til konsentrasjonen av oksoniumioner (H3O+) målt i mol per liter (mol/l).
pH = -log[H3O+]
H3O+ oppstår ved at H+-ioner reagerer med H2O, og for enkelhets skyld sier vi ofte H+ i stedet for H3O+. Det vil vi også gjøre her.
Hvis konsentrasjonen av H+ er 10-7 mol/l er pH-verdien 7. Hvis den er 10-6 mol/l, er pH-verdien 6 osv.
Denne skalaen ble funnet opp av den danske vitenskapsmannen Søren Sørenson i 1909. pH-skalaen går fra 0 til 14, der 7 er nøytral. Verdier som er høyere enn 7 er basiske, mens verdier under 7 er sure. Eddik har for eksempel pH ca 3, destillert vann har nøyaktig 7. Konsentrert vannløsning av bakepulver (natriumhydrogenkarbonat eller NaHCO3(aq)) har pH på 8,2. Noen rengjøringsprodukter som inneholder ammoniumhydroksid (NH4OH(aq)) har pH på 11-12 og lesket kalk (Ca(OH)2(aq)) har pH-verdien 12,4.
I rent vann er den eneste kilden til H+ denne reaksjonen:
H2O -><- H+ + OH-
flytende hydrogenion hydroksidion
vann
Pilene som peker i begge retninger betyr at reaksjonen er reversibel. En syre er et stoff som øker konsentrasjonen av H+ når det løses i vann. Jo mer H+ som tilføres, jo sterkere er syren og jo lavere er pH-verdien. |
Sur nedbør
Nedbør er vanligvis litt sur fordi karbondioksidet (CO2) som forekommer naturlig i lufta, oppløser seg i nedbøren. Det dannes en løsning av karbonsyre (H2CO3), slik at pH-verdien blir rundt 5,6. Dette skjer fordi noen av karbonsyremolekylene avgir hydrogenioner til vann så det dannes oksoniumioner. Tilbake blir hydrogenkarbonat:
|
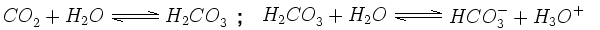 |
 |
|
I en mer basisk oppløsning med høyere pH, kan hydrogenkarbonat miste enda et hydrogenion og bli til karbonat. Mange steiner og sedimenter, f.eks. dolomitt eller kalkstein, består av karbonatsalter.
|
|
Men rent regn er litt surt, på grunn av karbonsyren. Vi snakker om sur nedbør når pH-verdien er under 5,6 (noen forskere setter grensa ved 5). Fordi også snø og tåke kan være surt, snakker vi generelt om sur nedbør.
Menneskenes bidrag til sur nedbør kommer fra svovel- og nitrogenforbindelser.
SO2 og NOx gjennomgår flere innviklete kjemiske reaksjoner før de blir til svovelsyre (H2SO4) og salpetersyre (HNO3), som man finner i sur nedbør.
|
 |
Svovelsyre kommer fra svovelforbindelser:
svoveldioksid og oksygen reagerer og danner svoveltrioksid:
2SO2 + O2 -> 2SO3
svoveltrioksid reagerer med vann og danner svovelsyre:
SO3 + H2O -> H2SO4
Salpetersyre kommer fra nitrogenoksider:
Nitrogendioksid og vann reagerer og danner salpetersyre og salpetersyrling:
2NO2 + H2O -> HNO3 + HNO2
|
|
En sur sky kan ha en pH-verdi så lav som 2,6. Sur nedbør i svært industrialiserte områder er vanligvis rundt 4,0; tåke i Los Angeles kan ha en pH på under 3,0. I noen områder i verden, som i nordlige Australia, kan organiske utslipp fra naturlig vegetasjon skape pH-verdier på rundt 4,4.
|
Årsak: Utslipp av SO2 og NOx
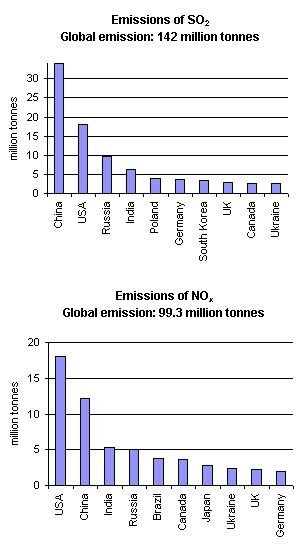
Hvorfor blir nedbøren sur? Den viktigste grunnen til at atmosfæriske syrer dannes i lufta, er kjemiske reaksjoner mellom syreframkallende gasser (SO2 og NOx) og vann. Mesteparten av SO2 og NOx slippes ut i atmosfæren ved forbrenning av fossilt brennstoff. Veitransport, skipsfart og luftfart er viktige kilder til utslipp NOx; naturlige kilder er blant annet vulkaner, lynnedslag og biologisk forråtnelse. Naturlige kilder til SO2 er vulkaner, havet (dimetylsulfid og COS), biologisk forråtnelse og skogbranner. Sur nedbør er imidlertid først og fremst et resultat av menneskeskapte utslipp. Figur 2 viser hvilke 10 land som står for de største utslippene av SO2 og NOx. I begge tilfeller er det USA, Kina, Russland og India som topper listen. Dette skyldes i stor grad høye innbyggertall, men i USA er også utslipp per innbygger svært høye, på grunn av det store energiforbruket.
|
 |
 |
 |
|
2. Utslipp av SO2 og NOx i 1995. Etter 1995 har SO2-utslippene i Europa og Nord-Amerika blitt redusert, mens de har økt i Asia.
Forfatter: Anita Bokwa
Kilde: World Resources Institute, Washington DC
http://earthtrends.wri.org
|
|
Usikkerhet om globale utslipp
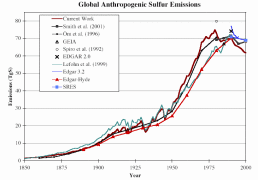
Det er stor usikkerhet involvert hvis man skal forsøke å lage en oversikt over de globale SO2- og NOx-utslippene. De naturlige utslippene av SO2 blir beregnet til å stå for 25-50% av de totale utslippene. I industrialiserte og urbaniserte områder, er imidlertid antropogene kilder beregnet til å stå for så mye som 90% av utslippene. Usikkerhetene varierer sterkt fra ett område til ett annet. Usikkerhetene kommer av mangel på data, spesielt om jordbruksforvaltning og usikre målinger for utslipp fra jord og vann. Figur 3 viser resultatene av forskjellige undersøkelser. Merk at figurene 3 og 4 viser verdiene for ren svovel, mens på figur 2 viser de svoveldioksid.
|
 |
 |
 |
|
3. Utviklingen i de globale menneskeskapte svovelutslippene. Flere undersøkelser sammenliknes og presenteres sammen i ett diagram.
Kilde: S. J. Smith, R. Andres, E. Conception, J. Lurz, 2004, Sulfur dioxide emissions: 1850-2000 (JGCRI Report. PNNL-14537)
Klikk for å forstørre!
|
|
|
Forandringer i utslippsmønstrene
Mennesker har doblet den naturlige utslipp av nitrogenforbindelser (N), og innholdet av atmosfærisk N har økt mellom tre til mer enn 10 ganger sammenliknet med før-industrielle tider. Utslipp av svovel (S) til atmosfæren er mer enn fordoblet.
|
 |
 |
|
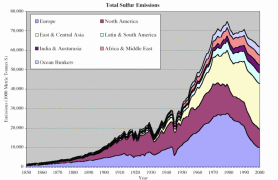
4. De viktigste økonomiske regionenes bidrag til menneskeskapte svovelutslipp siden 1850.
Kilde: S. J. Smith, R. Andres, E. Conception, J. Lurz, 2004, Sulfur dioxide emissions: 1850-2000 (JGCRI Report. PNNL-14537)
Forklaringer: Austurasia - Australia, New Zealand, South-Eastern Asia, Ocean Bunkers - fossil fuels used for ocean shipping
Klikk for å forstørre!
|
|
 |
Siden den industrielle revolusjon har Europa og Nord-Amerika stått for mesteparten av det menneskeskapte bidraget til svovelutslipp globalt. Det var imidlertid de økende utslippene i Øst- og Sentral-Asia som var den viktigste årsaken til det globale økningen av utslipp på 1970-tallet. Svoveldioksidutslipp i Europa økte allerede betraktelig på slutten av 1800-tallet, på grunn av industrialiseringen og økende forbruk av kull. Etter 1945 økte oljeforbruket svært raskt og utslipp av svovel ble doblet mellom slutten av krigen og begynnelsen av 70-tallet. |
|
I dag er sur nedbør et sterkt økende problem i Asia, med SO2-utslipp som ventes å tredobles fra 1990 til 2010 hvis den nåværende tendensen fortsetter. For å innskrenke de allerede betydelige skadene som skyldes sur nedbør og å unngå mye verre skader i framtiden vil det kreves investeringer på linje med dem som ble gjort i Europa og Nord-Amerika i løpet av de siste 20 årene. Utslipp av svoveldioksid i Europa er redusert med 44% i perioden fra 1990 til 1998. Utslipp av nitrogenoksider falt med 21% over den samme perioden. I USA og Canada var det en nedgang på 28% i SO2-utslipp mellom 1980 og 1995.
|
|
Utslippene er konsentrert i noen få regioner i verden. Øst-Asia slipper ut den største andelen SO2, mens USA slipper ut mest NOx.
|
Om denne siden:
Forfattere: Anita Bokwa - Jagiellonian University - Krakow / Polem, Elmar Uherek - Max Planck Institute - Mainz / Tyskland
Pedagogisk utprøving: Michael Seesing - University of Duisburg - Duisburg / Tyskland
sist oppdatert: 2004-08-17
|
|
 |
|







