|
|
 |
|
|
|
 |
| |
|
|
 |
Troposfera
Dowiedz się więcej! |
Występowanie i zawartość gazów atmosferycznych (2)
Gdy chcemy znać stężenia mniej trwałych związków chemicznych w atmosferze, nie wystarczy tylko podać jakąś cyfrę. Stężenia zależą bowiem w dużym stopniu od procesów chemicznych zachodzących w powietrzu.
|
|
|
|
|
 |
Profil pionowy
Zawartość gazów w powietrzu może być zróżnicowana w strefowo (w poziomie) w zależności od źródła ich pochodzenia, procesów pochłaniania i różnych parametrów fizycznych (dopływu światła słonecznego, temperatury, opadów, wiatru). Ale większość gazów wykazuje też różnice w zawartości w pionie. Często stosunek zmieszania maleje wraz ze wzrostem wysokości n.p.m., zwłaszcza nad tropopauzą i w warstwie dwóch kilometrów powyżej planetarnej warstwy granicznej (na którą bezpośrednio wpływa powierzchnia Ziemi), do wolnej troposfery. Wyjątkiem jest ozon, który ma najwyższy stosunek zmieszania i najwyższe stężenie w warstwie ozonowej w stratosferze. Ale nie musimy zaglądać aż tak wysoko. Większość procesów chemicznych ma miejsce w warstwie granicznej blisko powierzchni ziemi, gdzie emitowane są związki chemiczne.
Na wykresach poniżej można zobaczyć pionowe profile troposferyczne kilku organicznych i nieorganicznych gazów śladowych zmierzone przez samolot badawczy. Oprócz dwutlenku węgla, ozonu i metanu, typowe wielkości stosunku zmieszania to kilkaset ppt albo kilka ppb. Ale gazy widoczne tutaj należą do ważniejszych gazów śladowych, podczas gdy w atmosferze występują setki innych gazów organicznych, które mają niższy stosunek zmieszania, rzędu tylko kilku ppt.
|
 |
 |
 |
|
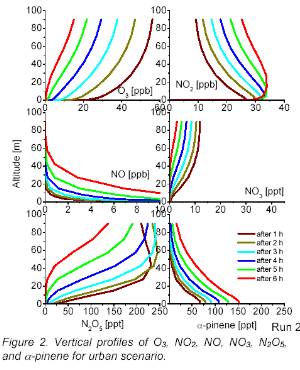
1. Zmiany stosunku zmieszania różnych związków chemicznych w ciągu nocy, blisko powierzchni ziemi. Wartości nie pochodzą z pomiarów, lecz są wynikiem zastosowania modelu chemicznego. Umożliwia on przy okazji wzięcie pod uwagę zmian w czasie, które są pokazane za pomocą różnych kolorów.
Autorzy: Andreas Geyer, Shuihui Wang i Jochen Stutz
Objaśnienia: altitude - wys. nad poziomem gruntu, after 1 h - po 1 godz., after 2 h - po 2 godz., itd.
|
|
|
|
 |
Zmierzone związki chemiczne:
CH4 = metan
CO = tlenek węgla
CH3OH = alkohol metylowy
CH3COCH3 = aceton
HCHO = formaldehyd
|
|
|
 |
O3 = ozon
NO = tlenek azotu
NOy = utlenione związki azotu bez NO, NO2
PAN = azotan nadtlenku acetylu
CN = jądra skroplenia (cząstki)
|
 |
 |
|
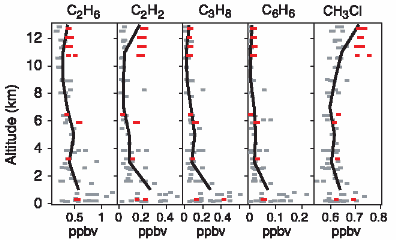
2. a- c) Pionowe profile zawartości różnych organicznych i kilku nieorganicznych gazów w powietrzu.
Wartości zostały zmierzone przez samolot badawczy nad Morzem Śródziemnym podczas akcji MINOS w sierpniu 2001. Grube czarne linie pokazują średnie wartości pionowych profili, cienkie czarne linie pokazują odchylenie standardowe. Szare kwadraty pokazują wartości wzięte z próbek z kanistrów. Czerwone linie kreskowe i czerwone kwadraty pochodzą z innego lotu i pozwalają nam zrozumieć, jak te wartości mogą zmienić się w ciągu kilku dni.
Każde powiększenie diagramu ma 16kb. Kliknij na ilustrację!
Dane i ilustracja: J. Lelieveld i współautorzy
|
|
 |
C2H6 = etan
C2H2 = acetylen = etyn
C3H8 = propan
C6H6 = benzen
CH3Cl = metylochloroform
|
Gazy w troposferze
Pełny przegląd gazów śladowych i ich stężeń w troposferze jest w zasadzie niemożliwy. Ten sam związek może występować w niezmiernie niskim stężeniu na przykład nad oceanem, i w bardzo wysokim stężeniu w środowisku miejskim. Poza tym, kilkadziesiąt gazów posiada duże znaczenie. Dlatego poniższa tabelka jest tylko zestawieniem przykładów i podaje najczęściej spotykany zakres stosunku zmieszania (zwykle blisko ziemi), dla często mierzonych związków.
|
|
Główne gazy w atmosferze:
|
nazwa |
wzór |
stosunek zmieszania |
azot |
N2 |
78,08 % |
tlen |
O2 |
20,95 % |
argon |
Ar |
0,93 % |
para wodna |
H2O |
0,1 - 4 %
= 1 000 - 40 000 ppm |
dwutlenek węgla |
CO2 |
372 ppm* |
tlenek węgla |
CO |
50 - 200 ppb |
metan |
CH4 |
1,7-1,8 ppm* |
wodór |
H2 |
0,5 ppm
(480 - 540 ppb) |
ozon |
O3 |
10 -100 ppb
średnia troposferyczna: 34* ppb |
rodnik hydroksylowy |
OH |
< 0,01 - 1 ppt |
dwutlenek azotu |
NO2 |
1 - 10 ppb |
tlenek azotu |
NO |
0,1 - 2 ppb |
podtlenek azotu |
N2O |
320 ppb* |
rodnik azotanowy |
NO3 |
5 - 450 ppt |
kwas azotowy |
HNO3 |
0,1-50 ppb |
amoniak |
NH3 |
< 0,02 - 100 ppb |
dwutlenek siarki |
SO2 |
1 ppb (w otoczeniu)
1 ppm (zanieczyszczone powietrze) |
formaldehyd |
HCHO |
0,5 - 75 ppb |
kwas mrówkowy |
HCOOH |
< 20 ppb |
aceton |
CH3COCH3 |
0,1 - 5 ppb |
izopren |
C5H8 |
< 1 - 50 ppb |
monoterpeny |
- |
< 100 ppt |
CFC11 |
CCl3F |
258* |
CFC12 |
CCl2F2 |
546* | |
* Gazy stosunkowo równomiernie występujące na kuli ziemskiej, których stężenia rosną w wyniku działalności człowieka. Dane z lat 2001-2003.
|
Stosunek zmieszania, stężenia i różne jednostki:
Ilości gazów często są podawane w różnych jednostkach:
dla stężeń: cząsteczki/cm3 albo µg/m3
dla stosunku zmieszania: ppt (pmol/mol), ppb (nmol/mol), ppm (µmol/mol), % (10 mmol/mol)
Stosunek zmieszania jest często bardziej pomocny dla naukowca, ponieważ, gdy powietrze unosi się i rozszerza, to jego objętość rośnie i zmienia się wtedy stężenie, ale stosunek zmieszania pozostaje taki sam.
Konwersja jednej jednostki na inną zależy od ciśnienia (= wysokość) i ciężaru cząsteczkowego. Jeśli robimy obliczenie dla powierzchni Ziemi przy normalnym ciśnieniu około 1 bara, możemy wyrazić całkowitą ilość cząsteczek na objętość powietrza w następujący sposób:
1 mol = 22,4 l = 6 x 1023 cząsteczek =>
1 cm3 = 2,7 x 1019 cząsteczek
1 dm3 = 1 l = 2,7 x 1022 cząsteczek
1 m3 = 2,7 x 1025 cząsteczek
Przykład obliczenia:
2 µg/m3 = 2x10-6 g/m3 NO2 jest typową wartością dla dwutlenku azotu na obszarze pozamiejskim.
ciężar cząsteczkowy M(NO2) = 46 g/mol
To oznacza: 2 x 10-6 g/m3 = 4,3 x 10-8 mol/m3 = 2,6 x 1016 cząstek/m3
Tak więc stosunek zmieszania wynosi około 2,7 x 1016 / 2,7 x 1025 = 10-9 = 1 ppb
Ponieważ ozon ma podobny ciężar cząsteczkowy, M(O3) = 48 g/mol, możemy z grubsza powiedzieć, że
2 µg/m3 ozonu = 1 ppb
To obliczenie jest właściwe tylko dla powierzchni Ziemi, gdzie żyjemy. Tak więc, aby zmierzyć dla przypadków smogu ozonowego na obszarach miejskich możemy teraz obliczyć:
120 µg/m3 = 60 ppb -> wysoki poziom
240 µg/m3 = 120 ppb -> bardzo wysoki poziom, wykluczone sporty, ryzyko dla zdrowia
360 µg/m3 = 180 ppb -> niezmiernie wysoki poziom, bardzo niebezpieczny dla układu oddechowego, należy pozostać w domu!
|
O tej stronie:
Autor: dr Elmar Uherek - Max Planck Institute for Chemistry, Moguncja, Niemcy
Recenzent: dr Rolf Sander - Max Planck Institute for Chemistry, Moguncja, Niemcy - 2004-05-18
Ostatnia aktualizacja: 2004-04-06
Tłumaczenie na język polski: mgr Jerzy Bojan, Zespół Szkół, Proszowice; dr Anita Bokwa, Uniwersytet Jagielloński, Kraków
|
|
 |
|







