|
|
 |
|
|
|
 |
 |
|
|
 |
Forschung B: Bildung von Aerosol - Rolle der Schwefelsäure
 Menge an Partikeln in der Luft Menge an Partikeln in der Luft
Wir haben im Teil Forschung A beschrieben, wie an einem gängigen Partikelmessgerät für die Luftüberwachung die feinen Partikel mit einem Durchmesser von kleiner als 10 µm gemessen werden.
|
|
Mit solchen Geräten können wir einen Überblick darüber gewinnen, welche Mengen an Partikel an welchen Standorten im ländlichen Raum, in der Umgebung einer Stadt und direkt in den Stadtzentren gemessen werden.
|
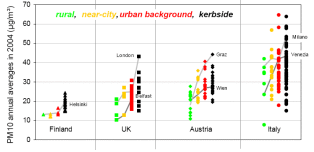
Die in den Stadtzentren (urban background) und direkt am Straßenrand (engl.: kerbside) gemessenen Konzentrationen sind in der Regel im Durchschnitt höher, als die in ländlichen (rural) und die Stadt umgebenden (near city) Regionen gemessenen Werte. Diese Unterschiede von der Stadt zur Stadtumgebung sind jedoch oft geringer, wenn die ganze Region stark belastet ist.
|
 |
 |
 |
|
1. PM 10 Jahresmittelwerte in verschiedenen Staaten Europas. Graue Linien verbinden Werte aus der gleichen Region vom umgebenden Land bis zum Straßenrand in der Stadt. Quelle: Jean-Philippe Putaud, JRC, and EEA/AIRBASE.
Bitte zum Vergrößern anklicken!
|
|
|
 Schwefelsäure und Partikelbildung Schwefelsäure und Partikelbildung
Aber auch in unbewohnten Gebieten gibt es immer eine bestimmte Konzentration an feinen Partikeln in der Luft. Für diese Partikel werden zwei Hauptquellen angenommen: Schwefelsäure und schwerflüchtige organische Verbindungen in der Luft. Auf dieser Seite sprechen wir nur über die Schwefelsäure.
|
 |
 |
|
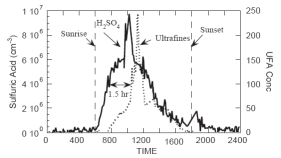
2. Zeitserie der Schwefelsäurewerte (schwarze Linie) bei anschließender Neubildung von Partikeln (gepunktet) am Idaho Hill, Colorado; 21. Sept. 1993 (Weber et al., 1997).
|
|
 |
Die Bildung von Sulfatverbindungen aus Schwefelsäure in der Luft führt zu sehr feinen Partikeln, die bei ihrer Entstehung meist unter den Erfassungsgrenzen der Messinstrumente liegen. Auf einer Feldmessung in den Rocky Mountains konnte gezeigt werden, dass die Bildung feinster Partikel einem Anstieg der Konzentration an Schwefelsäure (H2SO4) in der Atmosphäre folgt.* Dieser Anstieg ereignet sich vom Morgen zum Mittag.
|
|
Eine Partikelbildung kann dann erfolgen, wenn eine bestimmte Sättigung mit Schwefelsäure in der Luft erreicht ist und gleichzeitig eine gewisse Luftfeuchte vorliegt. Der kritische Punkt für die Partikelneubildung wird wesentlich eher erreicht, wenn in der Luft Spuren von Ammoniak (z.B. 1 ppt = Milliardstel Anteil) vorliegen. Denn dann kann die Schwefelsäure mit dem Ammoniak Ammoniumsulfatsalz bilden. Da Wasser als dritter Partner aber immer noch eine Rolle spielt, nennt man diese Art von Partikelbildung „ternäre Nukleation“ (Nukleation mit drei Partnern).
 Was beobachten wir bei einer Neubildung von Partikeln? Was beobachten wir bei einer Neubildung von Partikeln?
In der folgenden Bilderserie versuchen wir uns vorzustellen, was Forscher bei einer Partikelneubildung beobachten und was tatsächlich passieren kann.
|
 |
 |
|
Das wissen wir aber gar nicht genau. Es kann auch sein, dass die Schwefelsäure auf die schon vorhandenen Cluster aufgewachsen ist und sich sogar noch mit anderen Substanzen gemischt hat.
|
|
 |
Somit liegt der Geburtsmoment der Partikel für uns leider immer noch weitgehend im Dunkeln. Viele der neu gebildeten Partikel bleiben an größeren Partikeln haften, bevor sie so groß geworden sind, dass unsere Messinstrumente sie sehen. Je kleiner die Wachstumsraten der Partikel und je mehr größere Partikel schon in der Luft waren, desto unwahrscheinlicher ist es, ultrafeine Partikel im Bereich 3 - 20 nm zu beobachten.
Da wir aber ultrafeine Partikel im Labor aus Wasser und Schwefelsäure sehr gut herstellen können, nehmen wir an, dass sie sich auf diesem Wege auch in der Luft bilden.
|
|
 Chemie der Schwefelsäure-Bildung Chemie der Schwefelsäure-Bildung
Wir sehen in Abbildung 2, dass die Schwefelsäure zu einer bestimmten Tageszeit gebildet wird. Dieser Zusammenhang ist nicht verwunderlich. Schwefelsäure entsteht durch Oxidation von Schwefeldioxid. Die hierfür erforderlichen Sauerstoffverbindungen werden vor allem durch chemische Reaktionen erzeugt, die während des Tages von der Sonnenenergie angetrieben werden. Schwefeldioxid aber hat natürliche Quellen (Emissionen von Algen und Vulkanen) und wird heute auch in großen Mengen vom Menschen in die Atmosphäre entlassen (Verbrennung von Kohle und Schweröl, Industrieprozesse).
|
4. In der Atmosphäre bildet sich Schwefelsäure auf verschiedenen zum Teil recht komplexen Wegen, sowohl in der Gasphase als auch in der flüssigen Phase. Das Schema rechts zeigt zwei wichtige Wege, zum einen die Oxidation mit Hydroxi-Radikalen in der Gasphase, zum anderen die Oxidation mit Ozon (oder alternativ anderen Oxidantien) in der flüssigen Phase, d.h. in Wolkentropfen oder Nebel. Auch die Reaktion des Schwefeltrioxid (SO3) mit Wasser ist komplexer als in der einfachen Reaktionsgleichung. Es sind mehrere Wassermoleküle beteiligt.
Schema: Elmar Uherek; bitte zum Vergrößern anklicken!
|
 |
|
* Ein Problem der Aerosolforscher ist, dass diese feinsten Partikel zwar nachweisbar sind, ihre chemische Zusammensetzung jedoch nicht ermittelt werden kann, da die Substanzmengen zu klein sind. Die Theorie der Bildung neuer Partikel aus Schwefelsäure ist daher zwar schlüssig und allgemein anerkannt, aber nicht endgültig erwiesen.
|
|
 |
|







