|
|
 |
|
|
|
 |
| |
|
|
 |
Troposfera
Dowiedz się więcej! |
Ćwiczenie 2
Promieniowanie, pochłanianie i kolor
|
|
|
|
|
 |
 |
 |
|
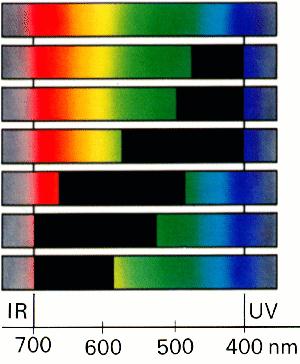
Rys. 1. Spektrum białego światła
© 2004 Seesing, Tausch; Universität Duisburg-Essen, Duisburg [Lit:Tausch, von Wachtendonk: Chemie SII, Buchner Verlag, Bamberg 1993]
|
|
Światło widzialne jest pewną częścią spektrum promieniowania elektromagnetycznego. Składa się z maleńkich jednostek energii nazywanych kwantami światła lub fotonami. Energia fotonu zależy od długości fali. Jeśli do naszych oczu dociera taka sama ilość fotonów z każdego przedziału długości fal spektrum widzialnego, to odbieramy to jako światło białe. Jeśli widzimy, że jakiś obiekt jest biały to znaczy, że odbija on równomiernie wszystkie fotony jakie składają się na światło białe. Używając pryzmatu lub siatki dyfrakcyjnej (np. na CD) możemy zobaczyć, że światło białe zostaje rozszczepione na poszczególne kolory, a ich uszeregowanie odpowiada ilości przenoszonej energii (patrz rys. 1). W przypadku pryzmatu przyczyną rozszczepienia jest refrakcja (załamywanie się promieni świetlnych), zaś w przypadku siatki – odbicie pod różnymi kątami.
Jeśli światło o danym zakresie fal jest pochłaniane to widzimy dopełniający kolor pochłanianego światła.
|
|
|
Z 1 |
Jaki kolor widoczny dla naszych oczu należy do poszczególnych zakresów fal? |
|
 |
 |
|
© 2004 Seesing, Tausch; Universität Duisburg-Essen, Duisburg [Lit:Tausch, von Wachtendonk: Chemie SII, Buchner Verlag, Bamberg 1993]
|
|
 |
|
|
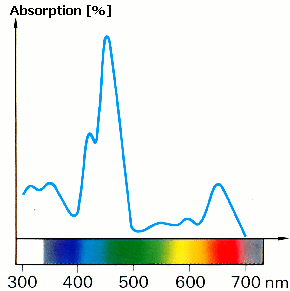
Większość obiektów wokół nas ma jakiś kolor. Większość z nich pochłania światło w kilku zakresach fal. Zazwyczaj absorpcja w poszczególnych zakresach nie jest jednakowo duża (patrz rys. 2). Każda substancja ma charakterystyczne spektra absorpcji, których można użyć do jej zidentyfikowania. Niemniej jednak mając dwie substancje składające się z tych samych komponentów może się czasem okazać, że jedna z nich jest jaśniejszego koloru niż druga. |
|
Z 2 |
Spróbuj wyjaśnić dlaczego z dwu próbek tej samej substancji jedna jest jaśniejsza niż druga. Uzasadnij swoją hipotezę. Narysuj spektrum „ciemniejszego” chlorofilu b na rys. 2. |
|
 |
 |
 |
|
Rys. 2. Spektrum absorpcji chlorofilu b
© Tausch, von Wachtendonk: Chemie SII, Buchner Verlag, Bamberg 1993
|
|
|
Podstawy spektrometrii
Spektroskopia jest używana do identyfikacji substancji. W laboratorium możesz badać różne substancje za pomocą fotometru (nazywanego także spektrometrem). Metoda ta jest także stosowana w pomiarach satelitarnych atmosfery ziemskiej (patrz też: spektrum atmosfery z satelity GOME na stronie ESPERE: pole tematyczne „Troposfera” – więcej, część 1, Metody pomiarowe)
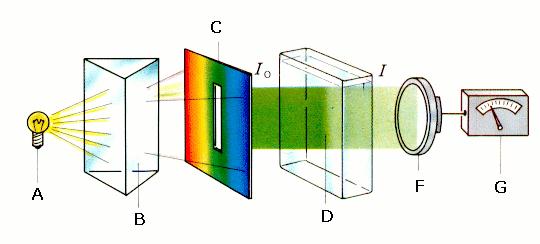
Fotometr składa się z elementów pokazanych na rys.3:
|
 |
 |
|
Rys. 3. Budowa fotometru
A: źródło światła; B: element monochromatyczny (pryzmat lub siatka dyfrakcyjna);
C: szczelina; D: naczynie z próbką; F: fotosensor; G: wzmacniacz ze skalibrowanym czytnikiem pokazującym OSŁABIENIE światła, Io: natężenie światła przed przejściem przez próbkę, I: natężenie światła po przejściu przez próbkę. Zmierzone OSŁABIENIE to stosunek natężenia światła, które przeszło przez próbkę (I) do pierwotnego natężenia światła (Io).
© 2004 Seesing, Tausch; Universität Duisburg-Essen, Duisburg [Lit:Tausch, von Wachtendonk: Chemie SII, Buchner Verlag, Bamberg 1993]
|
W zależności od stosowanej aparatury i dokładności pomiarów wyniki podaje się w procentach lub logarytmicznie.
|
 |
|
|
Wiele ustawień fotometru można zmieniać. Można używać różnych rodzajów lamp, zwłaszcza dla zakresu UV spektrum elektromagnetycznego, można zmieniać szerokość szczeliny, ustawienie elementu monochromatycznego (a zatem mierzone długości fal), temperaturę próbki, a także wielkość wzmocnienia. Można także zmieniać miąższość próbki poprzez dobór naczyń o różnych kształtach.
|
Z 3 |
Jakie ustawienia trzeba zmieniać z dużą dokładnością i w sposób ciągły aby otrzymać takie spektrum jak pokazane na rys. 2? Uzasadnij swoją odpowiedź. | |
|
Naukowcy Johann Heinrich Lambert (1728-1777) i August Beer (1825-1863) odkryli prawo, które nazwano od ich nazwisk prawem Lamberta i Beera:
|
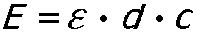 |
 |
|
E: osłabienie światła; ε: współczynnik osłabienia molowego (stała zależna od długości fal oraz substancji rozpuszczonych, jeśli były używane; d: miąższość próbki; c: stężenie substancji pochłaniających
|
|
Z 4 |
Podaj interpretację swojej hipotezy z Z 2 i zestaw ją z prawem Lamberta i Beera. Jaką proporcję (stosunek) nawiązującą do osłabienia promieniowania można eksperymentalnie udowodnić i wykorzystać? |
|
Z 5 |
Omów wyniki z Z 3 i Z 4! |
|
|
O tej stronie:
Autorzy: M. Seesing, M. Tausch - Universität Duisburg-Essen, Duisburg / Niemcy
Recenzent: Dr. Mark Lawrence - Max Planck Insitute for Chemistry, Moguncja, Niemcy - 2004-05-05
Ostatnia aktualizacja: 2004-05-13
Tłumaczenie na język polski: dr Anita Bokwa, Uniwersytet Jagielloński, Kraków |
|
 |
|







