|
|
 |
|
|
|
 |
| |
|
|
 |
Troposfera
Dowiedz się więcej! |
Procesy chemiczne zachodzące w atmosferze nocą
Procesy chemiczne zachodzące w atmosferze zależą nie tylko od rodzaju związków emitowanych do powietrza, ale także od warunków meteorologicznych. Te zaś zależą m.in. od pory roku i dnia, a określamy je opisując np. temperaturę czy wilgotność powietrza.
|
|
|
|
|
 |
 |
 |
|
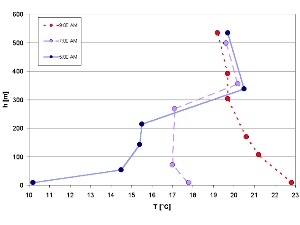
1. Zanikanie inwersji temperatury nad ranem w lipcu (pomiary z doliny Isar, Niemcy)
Autor: Elmar Uherek, na podstawie: Schirmer - Wetter und Klima - Wie funktioniert das?
Proszę kliknąć aby zobaczyć rycinę w powiększeniu (50 K)!
|
|
 |
Cykl dobowy
W poprzedniej części poznaliśmy dobowy cykl OH, który zależy od dopływu światła słonecznego. Jednak nie tylko związki chemiczne podlegają cyklom dobowym, to samo dotyczy własności atmosfery, np. pionowego profilu temperatury. Warunki panujące w planetarnej warstwie granicznej, blisko powierzchni ziemi, są bardzo zmienne i nie zawsze odpowiadają ogólnym regułom (np. że temperatura spada wraz ze wzrostem wysokości). Dzieje się tak wskutek wielu procesów zachodzących między planetarną warstwą graniczną a powierzchnią Ziemi. Typowym przykładem jest tworzenie się nocnej warstwy inwersyjnej, która zanika nad ranem.
|
Nocna inwersja temperatury w planetarnej warstwie granicznej
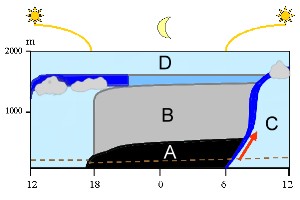
Masy powietrza znajdujące się poniżej swobodnej atmosfery (oznaczonej jako D na ryc. 2) należą do planetarnej warstwy granicznej. Zmiany niektórych jej cech zachodzą w ciągu doby (od lewej do prawej na ryc. 2): w południe powietrze jest wymieszane (kolor jasnoniebieski). Po zachodzie Słońca tworzy się w dolnej warstwie atmosfery nocna warstwa stałej równowagi atmosfery (A), a powyżej znajduje się nocna warstwa słabej turbulencji (B). Powietrze znajdujące się w warstwie przygruntowej (poniżej przerywanej brązowej linii) nie może w nocy przemieszczać się do wyższych warstw atmosfery. Brak energii słonecznej, która wyzwala ten proces. Nad ranem ziemia zaczyna się ogrzewać, powietrze zaczyna się unosić (czerwona strzałka), nocna warstwa stałej równowagi zaczyna zanikać. Tworzy się wąska tzw. strefa wznoszenia (ciemny niebieski kolor), która unosi się stopniowo aż do górnej granicy planetarnej warstwy granicznej i pozostawia poniżej w ciągu dnia konwekcyjną warstwę mieszania (C).
|
 |
 |
 |
|
2. Uproszczony model planetarnej warstwy granicznej. Miąższość tej warstwy jest zmienna. Objaśnienia w tekście.
Autor: Elmar Uherek, na podstawie: Stull 1988
Proszę kliknąć aby zobaczyć rycinę w powiększeniu! (70 K)
|
|
Zimą zdarza się, że Słońce jest zbyt nisko ponad horyzontem aby warstwa inwersyjna mogła zaniknąć. Utrzymuje się ona więc przez cały dzień, a nawet kilka dni. Jeśli ma to miejsce nad miastem to zanieczyszczenie powietrza gromadzi się w powietrzu i może to doprowadzić do powstania smogu. W górach zimą warunki meteorologiczne są szczególne, a inwersja może utrzymywać się np. pod warstwą chmur wypełniającą dolinę (ryc.3).
|
 |
 |
 |
|
3. Warstwa inwersyjna zimą w górach
© Inst. for geographical education, Univ. of Erlangen-Nürnberg
|
|
 |
 |
|
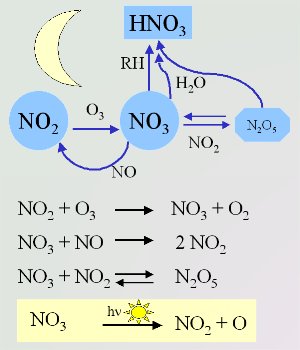
4. Najważniejsze reakcje chemiczne z udziałem azotu zachodzące w atmosferze w ciągu nocy. Fotoliza zachodząca w ciągu dnia pokazana jest w żółtym polu na dole ryciny.
Autor: Elmar Uherek
|
|
 |
Reakcje chemiczne z udziałem azotanów
To, że warunki meteorologiczne są w nocy inne niż w ciągu dnia powoduje, że procesy chemiczne zachodzące w atmosferze także są inne. Jest dostępne mniej źródeł OH, a rodniki azotanowe wchodzą w podobne reakcje z gatunkami organicznymi jak OH w ciągu dnia. Rodniki azotanowe NO3 tworzą się wskutek reakcji ozonu O3 z dwutlenkiem azotu NO2 (patrz: poziom „podstawy”, część 3). Następnie, przy udziale NO, zachodzi reakcja prowadząca do ponownego powstania NO2. To z tego powodu NO i NO3 nie mogą występować łącznie w wysokich stężeniach. Reakcja między NO3 i NO2 jest jedynym sposobem powstawania N2O5 w atmosferze. Może on albo ulec hydrolizie w wodzie albo rozpaść się z powrotem na NO2 i NO3.
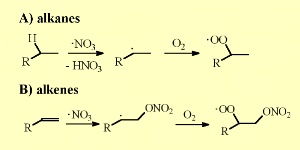
Podobnie jak OH, rodniki azotanowe odrywają atom H- od alkanów. Kwas azotowy HNO3 i rodniki alkilowe R tworzą się, a następnie reagują z tlenem zawartym w powietrzu i tworzą rodniki nadtlenowe RO2 tworzą się, a następnie reagują z tlenem zawartym w powietrzu i tworzą rodniki nadtlenowe RO2 . .
|
NO3 także dołącza się do podwójnych wiązań nienasyconych związków organicznych i tworzy azotany nadtlenowe po dodaniu O2. Co ciekawe, czas przebywania NO3 / N2O5 w atmosferze drastycznie spada wraz ze wzrostem zawartości pary wodnej. HNO3 tworzy się wskutek reakcji z wodą, zwłaszcza gdy jest to cienka jej warstwa na jakiejś powierzchni..
Wszystkie związki nadtlenowe, powstające w wyniku reakcji z udziałem  OH, NO3 lub ozonu, wchodzą w dalsze, liczne i skomplikowane reakcje w atmosferze z udziałem O2, HO2 OH, NO3 lub ozonu, wchodzą w dalsze, liczne i skomplikowane reakcje w atmosferze z udziałem O2, HO2 , RO2 , RO2 , NO lub NO2. Prowadzi to do powstawania m.in. alkoholi, aldehydów, azotanów i kwasów karboksylowych. Objaśnienie tych reakcji znacznie wykracza poza ramy niniejszej encyklopedii, zwłaszcza, że nie wszystkie są do końca poznane. , NO lub NO2. Prowadzi to do powstawania m.in. alkoholi, aldehydów, azotanów i kwasów karboksylowych. Objaśnienie tych reakcji znacznie wykracza poza ramy niniejszej encyklopedii, zwłaszcza, że nie wszystkie są do końca poznane.
|
 |
 |
 |
|
5. Reakcje azotanów z alkanami i alkenami.
Proszę kliknąć na rycinę aby zobaczyć ją w powiększeniu (30 K)!
|
|
 |
 |
|
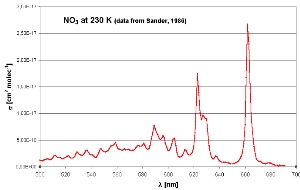
6. Zakres pochłaniania azotanów dla światła widzialnego. Maksimum w czerwonej części widma (600-700 nm).
Źródło: Sander (1986), zmienione. Pomiar w temperaturze 230 K.
|
|
 |
NO3 pochłania światło w czerwonej części widma widzialnego. Wraz z pierwszymi promieniami Słońca, ulega fotolizie głównie do NO2 i O, a reakcje z udziałem OH- ponownie dominują. Ozon, trzeci ważny utleniacz w atmosferze, nie jest w stanie reagować z alkanami, ale może stanowić konkurencję dla alkenów jeśli stężenie OH obniży się w warunkach niedoboru światła (zimą albo wieczorem). Reakcje z udziałem ozonu są opisane w osobnym tekście. |
|
Zajrzyj także na te strony!
Więcej informacji o tlenkach azotu w powietrzu:
Troposfera - podstawy - część 3 - NOx
|
O tej stronie:
Autor: dr Elmar Uherek - Max Planck Institute for Chemistry, Moguncja, Niemcy
Recenzent: Dr. Mark Lawrence - Max Planck Institute for Chemistry, Moguncja, Niemcy - 2004-05-05
Konsultacja dydaktyczna: Michael Seesing - Uni Duisburg, Niemcy - 2003-07-02
Ostatnia aktualizacja: 2004-05-07
Tłumaczenie na język polski: dr Anita Bokwa, Uniwersytet Jagielloński, Kraków
|
|
 |
|







