|
|
 |
|
|
|
 |
| |
|
|
 |
Troposfera
Wiadomości podstawowe |
Ozon w troposferze
Ozon jest prawdopodobnie najbardziej znanym gazem w klimatologii. Dlaczego?
Jest to bardzo "przekorny" gaz. Jest niezbędny w stratosferze, gdzie chroni nas przed szkodliwym promieniowaniem słonecznym UV. W troposferze jest jednak szkodliwy i wywołuje problemy zdrowotne. W niektórych wielkich miastach zdarza się, że zakazuje się używania samochodów, ponieważ istnieje niebezpieczeństwo przekroczenia wartości dopuszczalnych ozonu w atmosferze i powstania smogu ozonowego.
|
|
|
|
|
 |
|
Oprócz wywoływania niekorzystnego wpływu na zdrowie, ozon troposferyczny jest także silnym gazem cieplarnianym i przyczynia się do globalnego ocieplenia.
W tej części Encyklopedii przyjrzymy się, jak ozon przy powierzchni ziemi szkodzi roślinom i ludziom, działając także jako gaz cieplarniany. W temacie "Stratosfera" natomiast zobaczymy jak ozon chroni nas przed szkodliwym zakresem promieniowania ultrafioletowego.
|
1 a- e) trwałe uszkodzenie liścia jest typowym przykładem szkodliwego wpływu ozonu na roślinność. Na zdjęciach: Serotina Prunus (Czeremcha późna) uszkodzenie 0%, 4,4%, 7,8%, 12,3% i 24,5%.
Źródło: Innes, Skelly, Schaub-Ozon, Laubholz-und Krautpflanzen, ISBN 3-258-0638 4-2, Copyright by Haupt Verlag AG / Szwajcaria. Kliknij na zdjęcie, aby uzyskać powiększenie! (około 25 kB)
|
Ozon jest gazem o różnorakich właściwościach. Niektóre z nich są pożyteczne, a inne nie. Ozon występuje w różnych warstwach atmosfery. Warstwa ozonowa w stratosferze znajduje się na wysokości powyżej 10 km. Na tej właśnie wysokości ozon jest pożyteczny, bo pochłania szkodliwe zakresy UV i chroni nas przed rakiem skóry. Pewna niewielka ilość ozonu jest potrzebna także w troposferze, aby pomóc w procesach usuwania szkodliwych substancji chemicznych z powietrza. Niestety, w ostatnich dekadach stężenie ozonu w troposferze stale się powiększało. Czasami, w przypadkach wystąpienia smogu ozonowego, stężenie ozonu na pewnych obszarach bywa tak wysokie, że zagraża naszemu zdrowiu.
|
 |
 |
 |
|
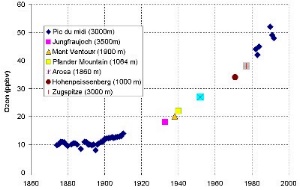
2. Ilość ozonu w troposferze nieprzerwanie rośnie od czasu pierwszych pomiarów w 1870 r. Wykres pokazuje poziom ozonu mierzony w ilości cząsteczek ozonu na jeden miliard cząsteczek powietrza objętościowo (ppbv).
Zestawione przez Valérie Gros, MPI, Moguncja, na podstawie: Marenco et al., 1992 (Long term evolution of ozone at the mid-latitudes of the Northern Hemisphere, European Geophysical Society, XVII General Assembly, 6-10.04.1992, Edynburg).
|
|
|
|
 |
Zagrożenie dla układu oddechowego
Ozon jest gazem reaktywnym i drażniącym, i w wysokich stężeniach prowadzi do problemów z układem oddechowym. Może spowodować zapalenie płuc i oskrzeli. Nasz organizm próbuje chronić przed ozonem pęcherzyki płucne. Jednak nie wchłanianie ozonu oznacza także dostarczanie mniejszych ilości tlenu. Mniej tlenu powoduje, że serce musi ciężej pracować. Narażeni na to ryzyko są przede wszystkim ci ludzie, którzy już mają problemy zdrowotne (np. astmę). W najgorszym wypadku ozon może stać się przyczyną śmierci.
|
Ozon: szczególna postać tlenu
Ozon jest szczególną postacią tlenu. Normalny tlen (O2) składa się dwóch atomów tlenu, natomiast ozon składa się trzech (O3), jest mniej trwały i bardziej reaktywny, można nawt powiedzieć agresywny. Ozon może powodować uszkodzenia tkanek organizmów żywych, co szerzej jest omówione w części "więcej", tekst 3. To dlatego ozon ma szkodliwy wpływ nie tylko na organizm ludzki, ale także na roślinność, jak pokazano na ilustracji 1.
|
 |
 |
 |
|
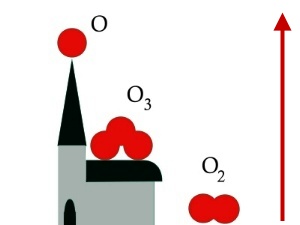
3. Trzy formy tlenu, ale o zupełnie różnej trwałości. Strzałka oznacza wzrastającą reaktywność.
Autor: Elmar Uherek
|
|
|
Postacie tlenu w powietrzu
|
postać tlenu |
liczba atomów |
trwałość chemiczna |
występowanie w powietrzu |
|
tlen atomowy |
1 atom |
nietrwały/bardzo reaktywny |
śladowe ilości |
|
"normalny" tlen |
2 atomy |
trwały |
21% powietrza |
|
ozon |
3 atomy |
raczej trwały/reaktywny |
10 - 100 ppb | |
ppb = części na miliard
|
Ozon jako gaz cieplarniany
Podobnie jak dwutlenek węgla (CO2) i metan (CH4), ozon troposferyczny pochłania promieniowanie cieplne docierające do atmosfery z powierzchni ziemi i przyczynia się do efektu cieplarnianego. Jest trzecim najważniejszym gazem cieplarnianym. Dodatkowe wymuszanie promieniowania 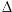 F mierzone od początków ery przemysłowej (około 1750 r.) jest miarą używaną po to, aby zbadać udział człowieka w ociepleniu Ziemi. Ryc. 4 pokazuje wpływ ozonu troposferycznego w porównaniu z innymi gazami cieplarnianymi. F mierzone od początków ery przemysłowej (około 1750 r.) jest miarą używaną po to, aby zbadać udział człowieka w ociepleniu Ziemi. Ryc. 4 pokazuje wpływ ozonu troposferycznego w porównaniu z innymi gazami cieplarnianymi.
Z tych właśnie przyczyn wysokie stężenia ozonu w troposferze są niepożądane.
|
 |
|
|
Oblicz udział gazów w globalnym ociepleniu!
Rycina 4 ukazuje udział kilku gazów cieplarnianych we wzroście wymuszenia promieniowania 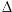 F przy tropopauzie podanym w Wm-2. Raport IPCC (rozdział 6.2.1 w "Podstawa naukowa") omawia zmiany średniej temperatury powierzchni Ziemi F przy tropopauzie podanym w Wm-2. Raport IPCC (rozdział 6.2.1 w "Podstawa naukowa") omawia zmiany średniej temperatury powierzchni Ziemi 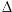 TS. Wzajemny stosunek obu parametrów z grubsza wygląda tak: TS. Wzajemny stosunek obu parametrów z grubsza wygląda tak:
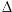 TS / TS / 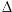 F = 0,5 °C / Wm-2 F = 0,5 °C / Wm-2
Czy potrafisz obliczyć zmianę temperatury 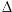 TS wywołaną przez dwutlenek węgla, metan, ozon i podtlenek azotu? TS wywołaną przez dwutlenek węgla, metan, ozon i podtlenek azotu?
|
O tej stronie:
Autor: dr Elmar Uherek - Max Planck Institute for Chemistry, Moguncja, Niemcy
Recenzent: dr Rolf von Kuhlmann, Max Planck Institute for Chemistry, Moguncja, Niemcy
Konsultacja dydaktyczna: Michael Seesing - University of Duisburg, Niemcy - 2003-07-02
Ostatnia aktualizacja: 2004-04-30
Tłumaczenie na język polski: mgr Jerzy Bojan, Zespół Szkół, Proszowice; dr Anita Bokwa, Uniwersytet Jagielloński, Kraków
|
|
 |
|







